Компоненты, из которых построено химическое соединение, еще со времени Лавуазье называются радикалами. Формально можно представить, что радикал является частью молекулы, получаемой отщеплением от нее водорода. Поэтому все радикалы содержат неспаренные электроны R: R1 → R + R1 и сами по себе неспособны существовать или существуют в течение ничтожных промежутков времени. Радикалы стремятся присоединить к себе атомы или группы и перейти в стабильное состояние. При таких превращениях радикалы, как правило, сохраняют неизменными все существовавшие в них связи между отдельными атомами.
В зависимости от числа образовавшихся неспаренных электронов, радикалы могут быть одновалентными, двухвалентными и т. д. От метана могут быть произведены радикалы
∙ СН3 ∙ 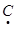 Н2 ∙
Н2 ∙ 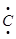 H
H
Доказательством существования этих радикалов является то, что первый из них — метил — может стабилизоваться путем присоединения другого метила, давая углеводород этана; второй образует соответственно этилен, а третий — ацетилен:
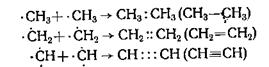
Третий процесс лежит в основе промышленного способа получения ацетилена из природного газа — метана.
Известны и неорганические радикалы. Так, при отщеплении атома водорода от молекулы воды образуется радикал ∙ОН. Радикалы содержат неспаренные электроны, но не несут электрического заряда.
К радикалам, с известной оговоркой, можно отнести простые газообразные вещества в атомарном состоянии, например атомарный водород, хлор и т. д.
Цепная реакция образования хлористого водорода протекает
через стадии образования свободных атомов (радикалов):
Cl2→ 2 ∙Cl
∙Cl + H2 → HCl + ∙H
∙H + Cl2 → HCl + ∙Cl и т. д.
Реакции, протекающие с образованием свободных радикалов, характеризуются большой скоростью и часто протекают взрывоподобно.
Радикалы имеют огромное значение в процессах полимеризации; их способность полимеризоваться используется в производстве синтетических каучуков и т. п. Взрывные реакции в двигателях внутреннего сгорания также протекают, с образованием свободных радикалов.
 2015-04-01
2015-04-01 790
790








