Рекуперационные методы очистки с регенерацией хемосорбентов
В этих процессах поглотитель регенерируют и повторно используют для очистки, а извлекаемый компонент перерабатывают в товарные серосодержащие продукты.
Для очистки отходящих газов от диоксида серы предложено большое количество хемосорбционных методов, однако на практике нашли применение лишь некоторые из них. Это связано с тем, что объемы отходящих газов велики, а концентрация в них SO2 мала, газы характеризуются высокой температурой и значительным содержанием пыли. Для абсорбции могут быть использованы вода, водные растворы и суспензии солей щелочных и щелочноземельных металлов.
Методы очистки дымовых газов от SO2
| метод | физико-химические свойства SO2, положенные в основу метода | продукты, полученные после обработки | абсорбент |
| известковый | способность SO2, как кислотообразующего окисла, давать с водой кислоту, легко вступающую в реакцию со щелочами | шлам, состоящий из сульфита и сульфата кальция (CaSO3 и CaSO4) | известняк, известь, мел |
| магнезитовый | – | 13 % SO2 (сернистый ангидрид), сульфат магния (MgSO3) | смесь магния |
| содо-цинковый | – | 100 % SO2 | окись цинка и соды |
| цинковый | – | – | окись цинка |
| каталитический | способность SO2 легко окисляться в соединения шести валентной серы | слабая (15 – 20 %) серная кислота H2SO4 | пиромозит (марганцевая руда) |
| аммиачный | способность SO2 образовывать со щелочами кислые соли (бисульфиты), которые являются неустойчивыми соединениями и разлагающимися при нагревании с выделением SO2 | 100 % SO2 и сульфат аммония | известь и пиромозит |
Известковый метод очистки дымовых газов от SO2
Наиболее широко применяемым является известковый метод. Достоинство: простая технология, низкие эксплуатационные затраты, доступность и дешевизна сорбента.
Процесс представляется в виде:
SO2 + H2O 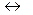 H2SO3;
H2SO3;
Ca(OH)2 + H2SO3 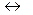 CaSO3
CaSO3 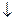 + 2H2O;
+ 2H2O;
CaSO3 + H2SO3 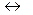 Ca(HSO3);
Ca(HSO3);
4CaSO3 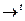 3CaSO4 + CaS;
3CaSO4 + CaS;
CaS + 2O2 = CaSO4.
Если H2SO3 постоянно нейтрализовать, то извлечение SO2 будет происходить с максимальной скоростью и 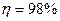 .
.
Схема очистки:
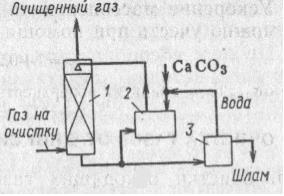
1 – абсорбер,
2 – сборник,
3 – вакуум-фильтр.
Предварительная очистка от пыли – выделение пыли в сухом виде, иначе пыль оседает в известковом растворе, что потребует фильтрации раствора (пыль будет влажной, что усложнит ее транспортировку с предприятия).
Отходы CaSO3 - применяют в бумажной промышленности для получения варочной кислоты для обработки целлюлозы. CaSO4 – гипс, вяжущее вещество, применяемое в строительстве.
Недостатки:
- большой расход извести, большое количество шлама, кристаллизация на стенках аппарата и газоходах.
Магнезитовый метод очистки дымовых газов от SO2
MgO + SO2 = MgSO3 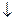 ; - сульфит магния
; - сульфит магния
MgSO3 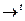 MgO + SO2 – реакция разложения
MgO + SO2 – реакция разложения
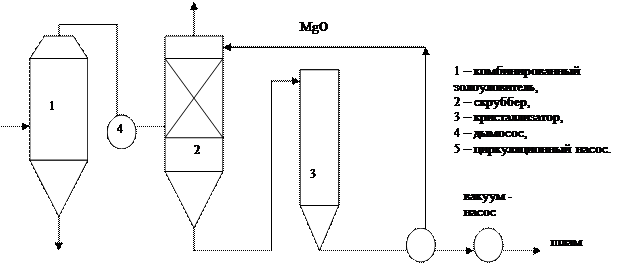
Газ перерабатывают в серную кислоту, а оксид магния возвращают на абсорбцию. В результате этого процесса достигается повышение концентрации SO2 с 0,3 до 13 %, что позволяет использовать его промышленно для получения H2SO4.
|
ГО
зола
Скруббер орошается раствором агрессивных солей Mg, поэтому поверхность скруббера выполняется в антикоррозийном исполнении. Сульфид Mg является солью малорастворимой и выпадает в осадок в виде крупных кристаллов Mg 6H2O. Некоторая часть (10 – 12%) MgSO3 окисляется в сульфат магния:
2MgSO3 + O2 = 2MgSO4;
этот процесс нежелателен при очистке, так как разлагается MgSO4 при очень высокой температуре (1000 – 1200 0С). Чтобы избежать образования MgSO4, необходимо сокращать время контакта фазы “газ - жидкость” или проводить процесс обжига сульфата в присутствии восстановителей (кокса, метана, оксида углерода). В этом случае MgSO4 восстанавливается в MgSO3. Часть раствора, орошающего скруббер, выводят из цикла орошения и направляют в кристаллизатор, где производится отделение кристаллов MgSO3. Кристаллы сульфита магния направляют на фильтрацию в вакуум – фильтры.
Раствор, отделенный от кристаллов, направляют в цикл орошения.
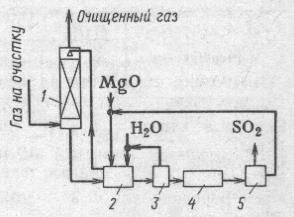 1 – абсорбер,
1 – абсорбер,
2 – нейтрализатор,
3 – центрифуга,
4 – сушилка,
5 – печь.
Из нейтрализатора часть суспензии выводят в центрифугу для отделения кристаллов солей магния. Обезвоживание солей производят в сушилках барабанного типа. Безводные кристаллы обжигают при температуре 900 0С, происходит реакция: MgSO3 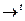 MgO + SO2. Концентрация SO2 в газе, выходящем из печи равна 7 – 15 %. Газ охлаждают, очищают от пыли и окиси магния и направляют на переработку в H2SO4. MgO охлаждают до температуры 120 0С, смешивают с водой и отправляют на абсорбцию.
MgO + SO2. Концентрация SO2 в газе, выходящем из печи равна 7 – 15 %. Газ охлаждают, очищают от пыли и окиси магния и направляют на переработку в H2SO4. MgO охлаждают до температуры 120 0С, смешивают с водой и отправляют на абсорбцию.
Достоинства метода:
- возможность очищать горячие газы без предварительного охлаждения;
- получение H2SO4;
- доступность и дешевизна сорбента;
- высокая эффективность очистки.
Недостатки метода:
- сложная технологическая схема;
- неполное разложение MgSO4 при обжиге;
- значительные потери MgO при регенерации.
Цинковый метод очистки дымовых газов от SO2
Абсорбент – суспензия оксида цинка:
SO2 + ZnO + 2,5H2O = ZnSO3 2,5H2O;
При большой концентрации O2 протекает следующая реакция:
2SO2 + ZnO + H2O = Zn(HSO3)2.
Образующийся сульфит цинка нерастворим в воде, его отделяют в гидроциклах, а затем сушат и обжигают при температуре 350 0С:
ZnSO3 2,5H2O 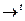 ZnO + SO2 + 2,5H2O.
ZnO + SO2 + 2,5H2O.
SO2 идет на переработку в H2SO4, а ZnO возвращают на абсорбцию.
Достоинства метода:
- возможность проводить процесс очистки при высокой температуре (200 - 250 0С).
Недостатки метода:
- сульфат цинка, образующийся в результате очистки экономически нецелесообразно подвергать регенерации, поэтому его необходимо непрерывно отводить из системы и добавлять в нее эквивалентное количество ZnO.
Аммиачный метод очистки дымовых газов от SO2
SO2 + 2NH3 + H2O = (NH4)2SO3 – сульфит аммония;
(NH4)2SO3 + SO2 + H2O 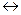 2NH4HSO3 – бисульфит аммония, неустойчивое соединение.
2NH4HSO3 – бисульфит аммония, неустойчивое соединение.
Метод может быть циклическим и нециклическим, тогда бисульфит аммония выпускают в качестве товарного продукта.
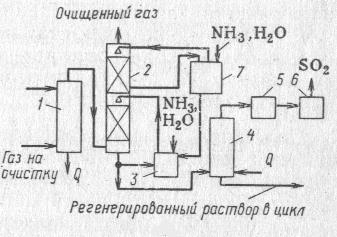
1 – колонна,
2 – абсорбер,
3 – емкость,
4 – отпарная колонна,
5 – конденсатор,
6 – осушитель,
7 – емкость.
Очистка отходящих газов от SO2 аммиачно – циклическим методом
Отличительной особенностью данного метода является поглощение диоксида серы SO2 водными растворами сульфит - бисульфита аммония при низкой температуре и выделение его при нагревании.
Выделенный при нагревании SO2 осушают и используют как товарный продукт высокого качества или перерабатывают в серу или серную кислоту. Раствор сульфита аммония охлаждают и вновь используют для абсорбции диоксида серы.
Схема очистки газов аммиачно – циклическим методом:
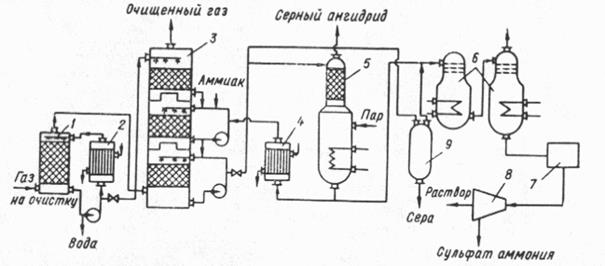 |
Отходящий газ после очистки от пыли поступает в скруббер 1, орошаемый водой при 30 0С, где поглощается 10 – 15 % SO2 от общего количества его в газе. Вода, циркулирующая в скруббере, охлаждается в холодильнике 2 и частично передается на орошение в башню 3, где поглощение SO2 осуществляется в несколько ступеней, суммарная степень очистки газа при этом составляет 90 %. Избыточный раствор из цикла орошения первой (нижней) ступени, содержащей наибольшее количество бисульфита аммония, непрерывно выводят из системы и направляют на регенерацию в отгонную колонну 5, обогреваемую глухим паром.
В отгонной колонне происходит разложение бисульфита аммония и частичное разложение других солей аммония с выделением SO2 и аммиака. Последний улавливается при конденсации паров воды.
Из отгонной колонны SO2 после конденсации паров воды и абсорбции аммиака поступает на сушку. Содержание его в сухом газе составляет 94 – 97 %.
Регенерированный в отгонной колонне раствор охлаждается в холодильнике 4 и вновь поступает в цикл орошения.
Для выделения из раствора сульфата аммония часть регенерированного раствора направляют в выпарные аппараты 6, а затем в кристаллизатор 7, где при охлаждении выпадают кристаллы сульфата аммония. Последние отжимают на центрифуге 8, а маточный раствор возвращают в цикл орошения абсорбера.
В поглотительном растворе может содержаться также тиосульфата аммония, поэтому часть раствора после абсорбера поступает в автоклав 9. Здесь под давлением и при температуре 140 0С сульфит, бисульфит и тиосульфат аммония разлагаются с образованием серы и подают в выпарные аппараты 6, а серу сливают в формы.
В цикл орошения постоянно добавляют аммиак, чтобы компенсировать его количество, расходуемое на образование сульфата аммония и потери в атмосферу.
Выделяемый продукт имеет следующий состав: 90 – 93 % (NH4)2SO4; 2 – 3 % (NH4)2SO3; 0,5 – 1 % NH4HSO3 и 4 – 5 % H2O.
Достоинства метода:
- получение 100 % SO2n(NH4) SO4 сульфата аммония (удобрение),
- степень очистки – 90 %.
Недостатки метода:
- зависимость степени очистки от атмосферных условий (t, 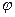 ),
),
- тщательный контроль процесса во избежание потерь аммиака,
- газы и жидкости имеют кислую реакцию, поэтому требуется антикоррозийная защита,
- большие эксплуатационные затраты и возможность очищать газы, содержащие SO2 более 0,3 %.
Есть схемы без предварительного охлаждения газа, по которым для реакции добавляют H2SO4:
(NH4)2SO3 + H2SO4 = (NH4)2SO4 + H2SO3.
Во Франции разработан метод аммиачно – бисульфитный, который позволяет очищать газы любого состава. В данном процессе сульфат аммония разлагается при температуре:
(NH4)2SO4 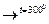 NH3 + NH4HSO4,
NH3 + NH4HSO4,
выделяется NH3 и бисульфат аммония возвращаются в процесс.
Недостаток: большая энергоемкость.
Схема очистки аммиачно - бисульфитным методом:
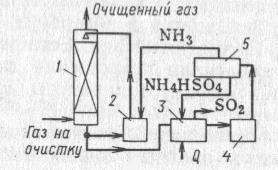 1 – абсорбер,
1 – абсорбер,
2 – емкость,
3 – отпарная колонна,
4 – узел выпаривания,
5 – сушилка.
Абсорбер, применяемый для улавливания SO2 должен быть высокой эффективности, иметь низкое гидравлическое сопротивление (до 3 кПа), малую металлоемкость, не забиваться осадками. Чаще всего применяются пустотелые скрубберы с форсунками и скрубберы Вентури одно - и двухступенчатые.
- не забиваться осадками, образующимися в процессе абсорбции.
Чаще всего используются пустотелые абсорберы с форсунками и скрубберы Вентури. Высокой эффективностью и простотой в эксплуатации обладает абсорбер типа СМ (рис. 5), сочетающий полую секцию с форсунками и секцию с барботажными
тарелками. 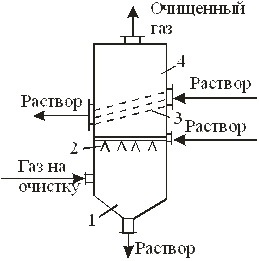
Рис. 4. Абсорбер типа СМ: 1 — секция очистки газа; 2 — форсунка;
3 — контактные тарелки; 4 — секция брызгоудаления
Исследуются также абсорберы с подвижной шаровой насадкой из полиэтилена или резины. Перспективными являются и абсорберы с крупнодырчатыми тарелками.
Мышьяково-содовый метод очистки дымовых газов от SO2.
Абсорбент приготавливают растворением мышьяка As2O3 в растворе Na2CO3 (NH4OH – мышьяково-аммиачный метод).
2As2O3 + H2O + 2Na2CO3  2NaHAs2O3 + 2CO2;
2NaHAs2O3 + 2CO2;
2Na2HAs2O3 + 5H2S  Na4As2S5 + 6H2O,
Na4As2S5 + 6H2O,
Na4As2S5 + O2  Na4As2S5O2
Na4As2S5O2
Раствор оксисульфомышьяково – натриевой соли является поглотительным раствором для сероводорода:
Na4As2S5O2 + H2S = Na4As2S6O + H2O.
При регенерации полученной соли кислородом воздуха выделяется сера:
2Na4As2S6O +O2 = 2Na4As2S5O2 + 2S.
Серу отделяют от раствора, а регенерационный раствор возвращают на абсорбцию.
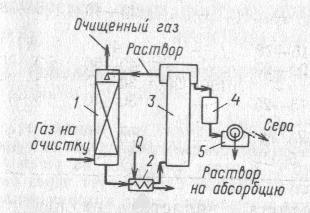 1 – колонна,
1 – колонна,
2 – теплообменник,
3 – колонна для окисления,
4 – емкость,5 – фильтр.
|
На процесс абсорбции влияет концентрация мышьяка. При увеличении концентрации с 15 до 25 г/л, эффект увеличивается с 81 до 97 %, рН = 7,8 – 7,9.
Недостаток метода:
- большой расход соды (400 – 500 кг на 1 гр серы),
- большое содержание примесей, что осложняет регенерацию.
Известен способ поглощения SO2 морской водой, которая имеет слабощелочную реакцию, за счет этого растворимость SO2 увеличивается.
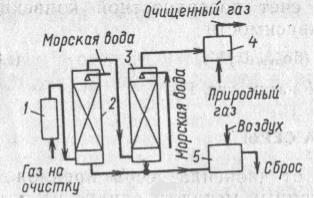 1 – электрофильтр,
1 – электрофильтр,
2, 3 – абсорберы,
4 – подогреватель,
5 - реактор
Газы очищают от золы, охлаждают в трубе Вентури, абсорбцию проводят в полом скруббере. Сточные воды после скруббера и абсорбера обрабатывают воздухом для окисления сульфитных соединений в сульфатные и сбрасываются в море (в Норвегии).
Очистка газов обжиговых печей от SO2
Метод основан на абсорбции SO2 известковым раствором в полых форсуночных аппаратах. Схема очистки
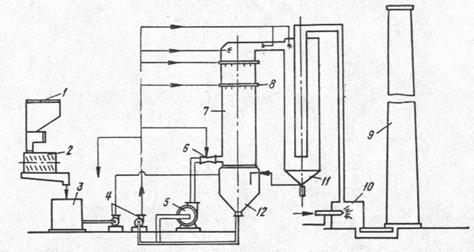 |
состоит из отделения подготовки поглотителя, двух газоочистных линий (одна резервная), включающих дымосос 5, полый форсуночный скруббер 7 с двухъярусным орошением, форсунки 8, систему обмыва стенок, каплеуловитель 11, подогреватель очищенных газов 10 и трубу рассеивания 9. Отходящие газы обжиговых печей, содержащие 30 – 45 г/нм3 SO3, предварительно обеспыливают в электрофильтрах, охлаждают до температуры 200 – 240 0С и дымососом 5 через сопло Вентури 6 подают на очистку в полый аппарат 7. Поглотительный известняковый раствор (суспензию) готовят в подготовительном отделении в аппаратах 1, 2, 3 и насосами 4 подают на орошение в сопло Вентури 6, в два яруса форсунок 8 и в систему обмыва стенок. Очищенный газ проходит каплеуловитель, подогреватель, после чего через 120 – метровую трубу рассеивания выбрасывается в атмосферу. Отработанную суспензию направляют в гидроциклоны, осветленную воду повторно используют для приготовления свежего раствора, а шлам после обезвоживания может быть использована как строительный материал.
Техническая характеристика работы установки:
количество газов, поступающих на очистку 50000 нм3/ч
температура 200 – 240 0С
запыленность газов 50 мг/нм3
содержание SO2 30 – 45 г/нм3
содержание SO3 до 5 г/нм3
степень очистки газов от SO2 и SO3 95 – 97 %
 2015-05-05
2015-05-05 8189
8189
