Связываются с аллостерическим центром фермента. Происходят изменения конформации аллостерического центра, а затем, через всю молекулу, они передаются на каталитический центр. Изменение конформации каталитического центра вызывает снижение активности фермента. Поэтому неконкурентные ингибиторы уменьшают Vmax - снижают скорость протекания II-го этапа ферментативного катализа. Не влияют на Km и не изменяют сродство фермента к субстрату.
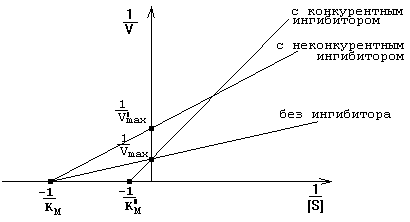
Действие обратимых ингибиторов на кинетические константы представлено на графике зависимости 1/V от 1/[S] (график Лайнуивера-Берка) - смотрите рисунок.
|
Измеряя скорость реакции при разных концентрациях субстрата в присутствии и в отсутствие ингибитора, можно не только распознать тип ингибирования, но и по степени изменения Км или Vmax количественно оценить степень сродства данного ингибитора к ферменту ("Ферменты", стр. 27-36).
 2015-04-20
2015-04-20 471
471








