С периодическими последовательностями сети реакций метаболизма кислот с коротким углеродным скелетом сопряжены две решетчатые формы. Эти формы представлены на рис.14 а,б.
Вертикальные колонки обеих решеток совпадают частично с интервалами последовательностей азотсодержащих соединений на рис.12 и с интервалами последовательностей, характеризующихся реакциями a-кетокислот на рис.13.б
Решетка на рис.14 а состоит из двух колонок. Колонки связаны между собой тремя обратимыми реакциями декарбоксилирования. В верхней реакции осуществляется превращение малоната в ацетат. Эта реакция играет ключевую роль в биосинтезе жирных кислот [25 с. 252-264]. Вторая реакция имеет значение как прямой путь превращения аспартата в аланин [224]. Третья реакция связывает оксалоацетат с пируватом [25 с. 314-322]. Эта реакция играет важную роль в метаболизме органических кислот (см. рис.10 и 11).
Решетка на рис.14 б состоит из трех колонок. Соединения ее левой колонки являются гомологами соответствующих соединений левой колонки решетки на рис.14 а, а соединения средней и правой колонок представляют собой изомерные гомологи соответствующих соединений правой колонки той же решетки. Левая и средняя колонки связаны между собой обратимыми реакциями декарбоксилирования, аналогичными реакциям декарбоксилирования решетки на рис.14 а. Средняя и правая колонки связаны сходными реакциями изомеризации. Верхняя пара реакций декарбоксилирования и изомеризации обычно рассматривается в связи с метаболизмом метилмалоната [25 с. 282-298]. Последний используется либо в биосинтезе разветвленных жирных кислот [149, 191], либо, превращаясь в
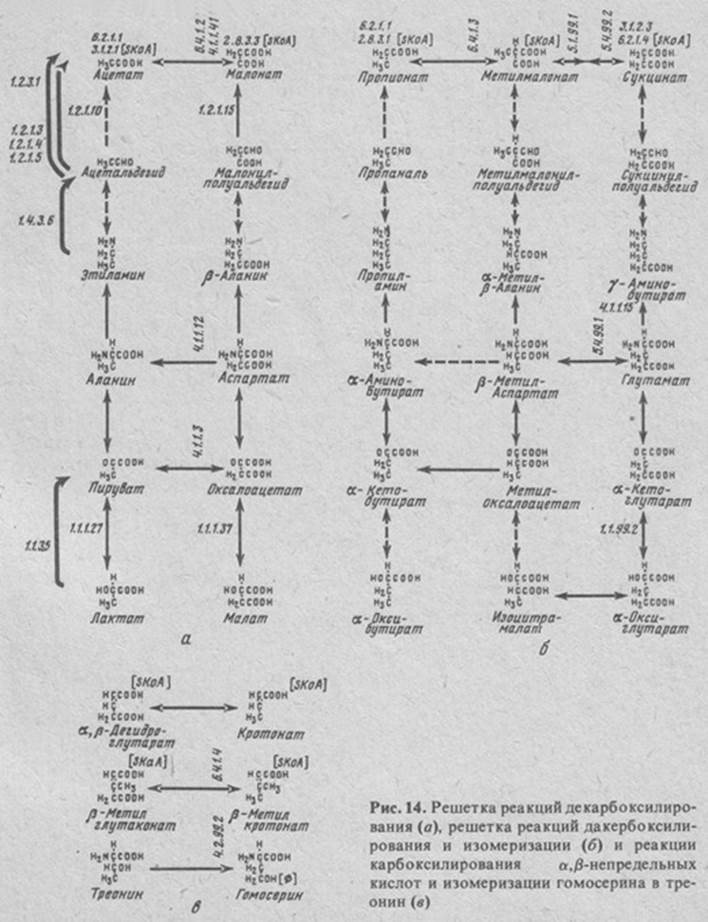
сукцинат, расщепляется в цикле Кребса. Реакции декарбоксилирования и изомеризации в нижней части рис.14 аналогичны верхним. Они обнаружены у бактерий [27 с. 181, 97].
Следует отметить еще три реакции, которые по своей природе близки к горизонтальным реакциям решеток, хотя и не входят в их число. К ним относится реакция карбоксилирования a,b-дегидроглутарата [288], сходная с ней реакция карбоксилирования b-метил кротоната [131, 253] и реакция изомеризации гомосерина в треонин [146, 147] (см. рис.14 а). Последняя реакция уникальна. С реакциями изомеризации на рис.14 б она имеет лишь формальное сходство. В отличие от них в этой реакции осуществляется изомеризация не углеродного скелета, а гидрокисльной группы.
 2015-05-06
2015-05-06 342
342








