1 2 3
P ¦ P2O5 ¦ Ca3(PO4)2 ¦ P
– CO
1) 8 2) 9 3) 11 4) 13 5) 19 6) 27
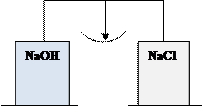
10. На чашах весов уравновешены стаканчики с растворами: левая чаша – гидроксида натрия, правая – хлорида натрия, через некоторое время …
1) стрелка весов отклонится влево
2) стрелка весов отклонится вправо
3) стрелка весов не изменит своего положения
4) раствор хлорида натрия изменит вкус
5) индикатор в растворе гидроксида натрия покажет щелочную среду
6) стрелка весов сделает скачок вправо, затем вернется в состояние равновесия
 |
влево вправо ®
Часть 3. Задания, оцениваемые в 5 баллов. В заданиях 11-15 установите соответствие между содержанием первого и второго столбцов. Впишите в таблицу ответы так, чтобы цифре первого столбца соответствовала буква из второго столбца.
11. Установите соответствие:
«МОЛЯРНАЯ КОНЦЕНТРАЦИЯ РАСТВОРА, моль/л – pH СРЕДЫ»
| 1) 0,1М HNO3 | А) 1 |
| 2) 0,01M HCl | B) 2 |
| 3) 0,1M KOH | C) 3 |
| 4) 0,01M KOH | D) 5 |
| 5) 0,001M НCl | E) 11 |
| F) 12 | |
| G) 13 |
12. Установите соответствие: «СХЕМА РЕАКЦИИ – общий КИНЕТИЧЕСКИЙ ПОРЯДОК РЕАКЦИИ»
| 1) A2 (газ) + B2 (газ) ¦ С(газ) | А) 0 |
| 2) A2 (газ) + B (тв) ¦ С(газ) | B) 1 |
| 3) A (тв) + B (тв) ¦ С(газ) | C) 2 |
| 4) A2 (газ) + 2B2 (газ) ¦ С(газ) | D) 3 |
| 5) 2A2 (газ) +3B2 (газ) ¦ С(тв) | E) 4 |
| F) 5 | |
| G) 6 |
13. Установите соответствие: «ГРАФИК ИЗМЕНЕНИЯ ЭНЕРГИИ ГИББСА химической реакции – ХАРАКТЕРИСТИКА РЕАКЦИИ»
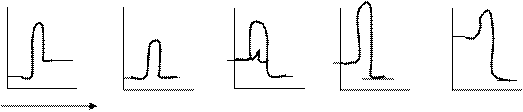 |
№1 №2 №3 №4 №5
ход реакции
| 1) №1 | А) эндотермическая |
| 2) №2 | B) идет очень быстро |
| 3) №3 | C) идет очень медленно |
| 4) №4 | D) находится в состоянии равновесия |
| 5) №5 | E) идет с участием катализатора |
| F) идет с участием ингибитора | |
| G) необратимая реакция |
14. Установите соответствие: «ТИП или СВОЙСТВО СОЕДИНЕНИЯ – ХИМИЧЕСКАЯ ФОРМУЛА»
| 1) кислая соль | А) Ni(CO)4 |
| 2) основная соль | B) Na2B4O7×10H2O |
| 3) двойная соль | C) KNaCl2 |
| 4) кристаллогидрат | D) (CuOH)2CO3 |
| 5) жидкое в о.у. соединение | E) (NH4)2Cr2O7 |
| F) NaAl(OH)4 | |
| G) HOOC – COONa |
15. Установите соответствие: «ОБРАЗЕЦ ВЕЩЕСТВА массой 10 г, растворяемого в 0,2 л воды – ЦВЕТ УНИВЕРСАЛЬНОГО ИНДИКАТОРА в растворе»
| 1) лёд | А) зелёный |
| 2) «сухой лёд» | B) голубой |
| 3) пищевая сода | C) желтый |
| 4) витамин С | D) оранжевый |
| 5) сок лимона | E) красный |
| F) бордовый | |
| G) «индиго» |
В заданиях 16-20 установите правильную последовательность. Запишите в таблицу буквы выбранных ответов рядом с номером задания (каждая буква пишется в отдельной клетке без пробелов и других символов, начиная с первой клетки).
16. Расположите химические формулы реагентов по порядку их следования в генетической цепочке превращений: 1,2,3,4,5
1 2 3 4 5
Cr(OH)3 ® NaCrO2 ® Na2CrO4 ® Na2Cr2O7 " CrО3 ® Cr2О3
1) NaOHр-р+H2O2р-р 2) NaOHтв 3) С2Н5ОН 4) HClразб. 5) H2SO4 конц.
17. Расположите характеристики дисперсных систем по порядку их следования: эмульсия, суспензия, аэрозоль, истинный раствор, коллоидный раствор:
1) видимые частицы жидкости распределены в газе
2) видимые частицы жидкости распределены в другой не растворяющей её жидкости
3) видимые твердые частицы распределены в жидкости
4) частицы дисперсной фазы не видны, т.к. их размер меньше 1 нм
5) частицы дисперсной фазы не видны, хотя их размер от 1 до 100 нм
18. Перечислите по порядку названия веществ, молекулы которых имеют указанные формы: угол, линия, треугольник, пирамида, «футбольный мяч»:
1) вода 2) аммиак 3) углекислый газ 4) С60 фуллерен 5) карбонат-ион
19. Расположите химические формулы солей в следующем порядке: не растворяется в воде; в растворе гидролиза нет; в растворе гидролиз по катиону; в растворе гидролиз по аниону; не существует в природе:
1) FeCl2
2) NaFeO2
3) FeS
4) Fe2S3
5) NaI
20. Укажите по порядку следствия влияния конкретных факторов изменения скорости реакции катализатор, температура, площадь соприкосновения фаз, концентрация веществ, природа веществ:
1) скорость реакции взаимодействия водорода с бромом увеличивается при нагревании
2) интенсивность реакции горения угля возрастает после его измельчения
3) скорость реакции разложения пероксида водорода увеличивается при внесении в него оксида марганца (IV)
4) скорость реакции горения фосфора повышается при внесении его в атмосферу чистого кислорода
5) водород выделяется быстрее в реакции между магнием и соляной кислотой, чем между цинком и соляной кислотой
Часть 4. Задания, оцениваемые в 6 баллов.
В заданиях 21-25 ответ записывается в таблицу ответов, начиная с первой клеточки. Каждая буква, цифра или символ пишется в отдельной клеточке, буквы должны быть печатными. Слова или числа при перечислении отделяются точкой с запятой. При записи ответов пробелы не используются. Фамилии указываются без инициалов в именительном падеже. Пропущенные слова записываются в именительном падеже, в единственном числе. Расчетные значения записываются без единиц измерения. Десятичные дроби заносятся через запятую.
21. Одиннадцатиклассник Взрывчик проверял на практике некоторые теоретические положения самостоятельно изученного им раздела химии, в котором рассматриваются вопросы скорости и механизма химической реакции. Эмпирическим путем юный химик исследовал химическую реакцию, уравнение которой u = k[A]x[B]y[C]z и установил, что если концентрация вещества А удваивается (при неизменных концентрациях веществ В и С), скорость реакции увеличивается в 8 раз; если концентрация вещества В удваивается (при неизменных концентрациях веществ А и С), скорость реакции возрастает в 2 раза; если концентрация вещества С удваивается (при неизменных концентрациях веществ А и В), скорость реакции возрастает в 4 раза.
В ответе должны быть указаны:
21.1. Значение показателей степени х, y (цифрами через запятую без пробела).
21.2. Значение показателя степени z и суммарный порядок реакции, которую исследовал юный химик (цифрами через запятую без пробела).
21.3. Название раздела химии, который изучал одиннадцатиклассник Взрывчик и фамилия одного из двух авторов закона, на основании которого смелый экспериментатор вывел уравнение изученной им реакции.
22. Эту головоломку юный химик Взрывчик придумал для химического КВНа: расположите в кружках знаки химических элементов из малых периодов, чтобы сумма их порядковых номеров в ПСХЭ по сторонам треугольника была одинакова.
Внимание! Знаки химических элементов не повторяются!
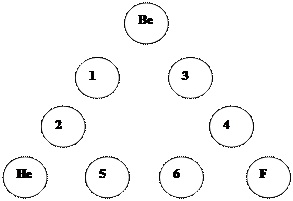 В ответе должны быть указаны по два угаданных химических символа через запятую без пробела:
В ответе должны быть указаны по два угаданных химических символа через запятую без пробела:
22.1. Знаки химических элементов 1,2.
22.2. Знаки химических элементов 3,4.
22.3. Знаки химических элементов 5,6.
23. У первоклассника Оксигенкина, приятеля юного химика Взрывчика, есть хобби – придумывать логические задачки. Вот одна из них: головоломка-полисиллогизм или сорит (такие задачки попадались Оксигенкину в книжке известного писателя Льюиса Кэррола «История с узелками», но Оксигенкин придумал свою задачку с химическим содержанием): прочитайте несколько утверждений, не связанных друг с другом, выделите общие слова и сделайте новый логически обоснованный вывод.
 2015-04-20
2015-04-20 1246
1246







