Метод основан на измерении электропроводности жидкости при изменении концентрации находящихся в ней солей.
Водные растворы являются проводниками второго рода – электролиты.
При диссоциации находящихся в жидкости веществ образуются (-) и (+) ионы, которые и являются носителями заряда.
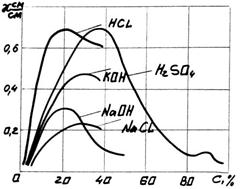
Степень диссоциации веществ находящихся в жидкости зависит от концентрации этих веществ. При высоких концентрациях степень диссоциации снижается. А это значит, что снижается и электропроводность жидкости. Максимальная электропроводность в растворах солей, кислот и щелочей наблюдается при концентрации от 15-25%. Поэтому при установке прибора измеряющего концентрацию необходимо выяснить уровень или требуемый диапазон.
Существует проблема измерения электропроводности раствора слабой концентрации. Т.к. на электропроводность оказывает влияние не только контролируемое вещество но и различные примеси.
Существуют электродные кондуктометры и безэлектродные.
Безэлектродные – для измерения концентрации агрессивных жидкостей.
Электродные – содержат 2 электрода, выполненных в виде электропроводящих пластин, помещённых в контролируемую жидкость. При изменении концентрации раствора изменяется ток в измерительной цепи. При питании кондуктометра постоянным током вблизи поверхности электродов скапливаются ионы противоположных знаков – поляризация. Поляризация электродов приводит к погрешности измерения. Для уменьшения погрешности применяются кондуктометры переменного тока.
В промышленности – 50 Гц.
В лабораторных условиях – 1-2 Кгц.
В качестве измерительной цепи применяются измерительные мосты. Кондуктометры включаются в одно из плеч моста.
 2015-04-20
2015-04-20 1133
1133








