189. Задание {{ 249 }} 150 Тема 1-0-0
Для фермента обладающего абсолютной специфичностью, характерно:
£ катализирует один тип реакции с несколькими субстратами
£ имеет конфигурацию активного центра способного подвергнуться небольшим изменениям
R способен катализировать только одну реакцию
£ радикалы активного центра способны взаимодействовать со стереоизомерами
190. Задание {{ 250 }} 151 Тема 1-0-0
Субстратная специфичность обуславливается:
£ определенными функциональными группами в активном центре
£ химическим соответствием активного центра субстрату
£ наличием кофермента
R комплиментарностью активного центра субстрату
191. Задание {{ 251 }} 152 Тема 1-0-0
Активность ферментов зависит от разрушения в первую очередь их:
£ первичной структуры
R третичной
£ вторичной
£ четвертичной
192. Задание {{ 252 }} 153 Тема 1-0-0
Для каталитической активности ферментов необходимо наличие...:
Правильные варианты ответа: кофермента;
193. Задание {{ 253 }} 154 Тема 1-0-0
Ионы Fe2+, Mn2+, Zn2+ играют роль...:
Правильные варианты ответа: кофакторов;
194. Задание {{ 254 }} 155 Тема 1-0-0
Когда кофермент связан с белком прочно и постоянно, его называют...:
Правильные варианты ответа: простетической группой;
195. Задание {{ 255 }} 156 Тема 1-0-0
Фермент гидролизующий мочевину называется:
£ аргиназой
R уреазой
£ глутамазой
£ цистениазой
196. Задание {{ 256 }} 157 Тема 1-0-0
Оксидоредуктазы - это ферменты катализирующие:
£ реакции гидролиза
£ реакции переноса групп
R окислительно-восстановительные реакции
£ реакции образования новых связей (С-С, C-O, С-N и т.д.)
197. Задание {{ 257 }} 159 Тема 1-0-0
Оптимальные условия действия амилазы pH=6,8, t=37. При изменении pH на 5, а t на 70:
R активность уменьшится
£ активность останется прежней
£ снижения pH ускорит реакцию
£ увеличение t0 уменьшит активность фермента
198. Задание {{ 258 }} 160 Тема 1-0-0
Если субстратом является сахароза Km=0,05мм, если рафиноза - Km=8мм. Скорость гидролиза выше в случае:
R сахарозы
£ рафинозы
£ обе миним
£ обе равны
199. Задание {{ 259 }} 162 Тема 1-0-0
Групповая специфичность определяется:
£ строением кофермента
R строением субстрата
£ витамином входящим в кофермент
£ апоферментом
200. Задание {{ 260 }} 166 Тема 1-0-0
Если фермент имеет 2 субстрата, то константа Михаэлеса для разных субстратов будет:
£ относится как 1:2
£ характеризует поведение фермента относительно к субстрату
£ одинаковые
R разные
201. Задание {{ 261 }} 167 Тема 1-0-0
Оптимальное значение pH действия фермента:
£ имеет постоянную величину
R свою область, область оптимальных значений
£ pH > 7 (щелочные)
£ pH < 7 (кислая)
202. Задание {{ 262 }} 168 Тема 1-0-0
Оптимальная температура действия основного большинства ферментов:
R 37-40
£ 0-10
£ 70-100
£ 70
203. Задание {{ 263 }} 169 Тема 1-0-0
Исследование субстратной специфичности, а также ингибирования ферментов дают информацию о строении:
£ аностеричексого центра
R активного центра
£ белковой части фермента
£ фермента в целом
204. Задание {{ 264 }} 170 Тема 1-0-0
Ингибиторы - вещества:
R подавляющие действие ферментов за счет того, что занимают активный центр (необратимые)
£ подавляют действие ферментов сорбируясь на аллостерическом центре
£ вызывают конформационные изменения активного центра
£ не подпускают субстрат к ферменту
205. Задание {{ 265 }} 171 Тема 1-0-0
Необратимые ингибиторы:
R связываются с активным центром
£ связываются с аллостерическим центром вызывая конформационные изменения в молекулы фермента
£ связываются с белковой частью фермента
£ вызывает конформационные изменения на растоянии
206. Задание {{ 266 }} 172 Тема 1-0-0
Обратимое конкурентное ингибирование - это когда:
R повышение концентрации субстрата устраняет или ослабляет ингибирование
£ повышение концентрации субстрата не влияет на результат ингибирования
£ субстрат и ингибитор атакуют оба активный центр, т.к. сходны по строению
£ атакует аллостерический центр и ингибитор перекрывает доступ субстрата к активному центру
207. Задание {{ 267 }} 173 Тема 1-0-0
Обратимый конкурентный ингибитор:
R связываемся с активным центром, но не гидрализуется
£ действует на активный центр, изменяя его конфигурацию
£ разрушает функциональные группы активного центра
£ сорбируется на аллостерическом центре
208. Задание {{ 268 }} 174 Тема 1-0-0
Неконкурентные ингибиторы присоединяются:
£ не к активному центру
R присоединяются в другом месте при этом конформации молекулы фермента изменяется
£ не в аллостерическом центре
£ не присоединяются вообще, а лишь влияет на изменение конформации
209. Задание {{ 269 }} 175 Тема 1-0-0
Регуляторный фермент - это фермент, задающий скорость, т.к. он катализирует... реакцию:
Правильные варианты ответа: лимитирующую;
210. Задание {{ 270 }} 176 Тема 1-0-0
Гомотропными называют аллостерические ферменты, у которых модуляторы - те же....
Правильные варианты ответа: субстраты;
211. Задание {{ 271 }} 177 Тема 1-0-0
Гетеротропные аллостерические ферменты - это те, у которых модулятор и субстрат:
Правильные варианты ответа: разные вещества;
212. Задание {{ 272 }} ТЗ № 97
Отметьте правильный ответ
Km – (константа Михаэлиса) – концентрация субстрата, при которой скорость равна:
£ ½ Vmax
£ 3/2 Vmax
£ ¼ Vmax
213. Задание {{ 273 }} ТЗ № 98
Отметьте правильный ответ
Скорость реакции:


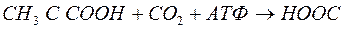 – С –СH2
– С –СH2 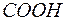 + АДФ+H3PO4
+ АДФ+H3PO4


O O
при уменьшении CO2
£ увеличится
£ не изменится
R уменьшится
£ концентрация CO2 не играет роли
214. Задание {{ 274 }} ТЗ № 99
Отметьте правильный ответ
На скорость ферментативной реакции оказывает влияние концентрация субстрата. Скорость будет максимальной, когда фермент (E) перейдет в [ES]:
R весь
£ ½ E
£ 3/4E
£ 2/5 E
215. Задание {{ 275 }} ТЗ № 100
Отметьте правильный ответ
На графике построенном по уравнению Лайнуивера-Берка на оси абсцисс отсекается отрезок равный
£ 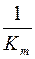
£ 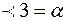
£ 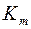
216. Задание {{ 276 }} ТЗ № 101
Отметьте правильный ответ
На оси ординат в графике построенном по уравнению Лайнуивера-Берка прямая отсекает отрезок равный:
£ 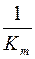
R 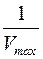
£ 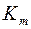
£ 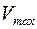
Белки
217. Задание {{ 20 }} 29 Тема 1-0-0
В триптофане радикал:
£ гидрофильный с анионной группой
£ гидрофильный с катионной группой
£ гидрофильный незаряженный
R гидрофобный
218. Задание {{ 21 }} 30 Тема 1-0-0
В аспарагиновой кислоте радикал:
R гидрофильный с анионной группой
£ гидрофильный с катионной группой
£ гидрофильный незаряженный
£ гидрофобный
219. Задание {{ 22 }} 31 Тема 1-0-0
В серине радикал:
£ гидрофильный с анионной группой
£ гидрофильный с катионной группой
R гидрофильный незаряженный
£ гидрофобный
220. Задание {{ 23 }} 32 Тема 1-0-0
В аргинине:
£ гидрофильный с анионной группой
R гидрофильный с катионной группой
£ гидрофильный незаряженный
£ гидрофобный
221. Задание {{ 24 }} 33 Тема 1-0-0
К аминокислотам содержащим гидрофобный радикал относятся:
£ лизин
£ глутамин
£ серин
R фенилаламин
222. Задание {{ 25 }} 34 Тема 1-0-0
К аминокислотам с гидрофильным незаряженным радикалом относятся:
R тирозин
£ метионин
£ пролин
£ лизин
223. Задание {{ 26 }} 35 Тема 1-0-0
Гидрофильный радикал с анионной группой содержит аминокислота:
£ цистин
R глутаминовая
£ серин
£ метионин
224. Задание {{ 27 }} 36 Тема 1-0-0
Гидрофильный радикал с катионной группой содержит аминокислота:
R гистидин
£ фенилаланин
£ аспарагин
£ изолейцин
225. Задание {{ 28 }} 37 Тема 1-0-0
Наличие пептидной связи в белке обнаруживается с помощью реакции
£ ксантопротеиновой
£ Сакагучи
£ Милоша
R биуретовой
226. Задание {{ 29 }} 38 Тема 1-0-0
Наличие остатка тирозина, триптофана, фенилаланина можно обнаружить с помощью реакции:
R ксантопротеиновой
£ Милоша
£ Сакагучи
£ Фоля
227. Задание {{ 30 }} 39 Тема 1-0-0
Какая из цветных реакций будет положительна с пептидом: Глу-Тир-Про-Арг
R биуретовая
£ Сакагучи
£ Фоля
£ Адамкевича
228. Задание {{ 31 }} 40 Тема 1-0-0
Какая цветная реакция будет положительна с пептидом: Три-Гли-Лей-Сер
R биуретовая
£ Фоля
£ Милоша
R Адамкевича
229. Задание {{ 32 }} 41 Тема 1-0-0
Щавелевоуксусная кислота образуется из аспарагиновой в результате реакции:
£ декарбоксилирования
£ элиминирования
R трансаминирования
£ альдольного расщепления
230. Задание {{ 33 }} 42 Тема 1-0-0
Серин превращается в пировиноградную кислоту в результате реакции:
£ трансаминирования
£ окислительного дезаминирования
R прямого дезаминирования
£ альдольного расщепления
231. Задание {{ 34 }} 43 Тема 1-0-0
Серин превращается в глицин в результате реакции:
£ декарбоксилирования
R альдольного расщепления
£ элиминирования
£ рацемизации
232. Задание {{ 35 }} 44 Тема 1-0-0
Глутаминовая кислота превращается в альфа-кетоглутаровую в результате реакции:
R окислительного дезаминирования
£ прямого дезаминирования
£ альдольного расщепления
£ рацемизации
233. Задание {{ 36 }} 45 Тема 1-0-0
Для обнаружения альфа-аминокислот используют реакцию:
£ ксантопротеиновую
R нингидринную
£ Адамкевича
£ Фоля
234. Задание {{ 37 }} 46 Тема 1-0-0
Гемоглобин выполняет в организме функцию:
R транспортную
£ защитную
£ структурную
£ регуляторную
235. Задание {{ 38 }} 47 Тема 1-0-0
Инсулин, репрессоры выполняют в организме функцию:
£ сократительную
£ защитную
£ структурную
R регуляторную
236. Задание {{ 39 }} 48 Тема 1-0-0
Водородные связи между пептидными группировками стабилизируют:
£ первичную структуру
R вторичную структуру
£ третичную структуру
£ четвертичную структуру
237. Задание {{ 62 }} ТЗ № 62
Отметьте правильный ответ
Аминокислота НООС ¾ СН ¾ СH2 COOH имеет тривиальное название:
½
NH2
£ аспарагин
£ глутамин
£ глутаровая
R аспарагиновая
239. Задание {{ 64 }} ТЗ № 64
Отметьте правильный ответ
Аминокислота НОСН2 ¾ СН ¾ COOH называется:
½
NH2
R серин
£ цистеин
£ лицин
£ аланин
240. Задание {{ 65 }} ТЗ № 65
Отметьте правильный ответ
Аминокислота H2N¾ (CH2)4¾CH ¾ COOH называется
½
NH2
£ аргинин
£ орнитин
R лизин
£ глутамин
241. Задание {{ 66 }} ТЗ № 66
Отметьте правильный ответ
Аминокислота СH3¾ CH¾CH ¾ COOH называется
½ ½
СН3 NH2
R валин
£ пролейцин
£ аланин
242. Задание {{ 67 }} ТЗ № 67
Отметьте правильный ответ
Аминокислота H2N¾C¾ NH¾ (CH2)3¾CH ¾ COOH называется
½½ ½
NН NH2
£ лизин
£ глутамин
£ аспарагин
R аргинин
 2015-04-30
2015-04-30 1628
1628
