ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ИЖЕВСКАЯ ГОСУДАРСТВЕННАЯ СЕЛЬСКОХОЗЯЙСТВЕННАЯ АКАДЕМИЯ»
КАФЕДРА ФИЗИКИ
Лаборатория оптики и физики атома «2 (012)
РАБОТА № 11
ИЗУЧЕНИЕ СПЕКТРА ИЗЛУЧЕНИЯ НЕОНА
Составители: профессор Ульянов
ассистент Воронцова Е.Н.
Ижевск, 2011
РАБОТА № 11
ИЗУЧЕНИЕ СПЕКТРА ИЗЛУЧЕНИЯ НЕОНА
Приборы и принадлежности: 1) спектроскоп УМ-2, 2) ртутная лампа, 3) неоновая лампа.
Раскаленные одноатомные газы и пары излучают линейчатые спектры, которые состоят из нескольких отдельно стоящих цветных линии на черном фоне. Атомы всех химических элементов имеют свой "спектроскопический портрет", то есть имеют присущие только данному элементу набор цветных линий в спектре. Например, натрий имеет две близко расположенные линии в желтой области спектра, водород – три, две из которых находятся в синей части спектра и одна в оранжевой.
Спектры многоатомных газов и паров состоят из ряда широких полос, это- молекулярные спектры. Наблюдения с помощью спектроскопов высокого разрешения показывают, что полосы молекулярных спектров состоят из отдельных линий.
Линейчатые спектры испускания от раскалённых одноатомных газов и паров наиболее полно объясняются с точки зрения квантовой механики. Согласно представлениям квантовой механики свет - это поток микрочастиц - фотонов, которые обладают одновременно и волновыми и корпускулярными свойствами. Волновые свойства проявляются при распространении света (явления дифракции, интерференции, поляризации). Корпускулярные свойства проявляются в процессе взаимодействия света с веществом (внешний фотоэффект, эффект Комптона), а также в процессах испускания света. Энергия частицы света - фотона EФ равна:
EФ = hν.
Здесь h = 6,6×10-34 Дж×с. – постоянная Планка,ν - частота света. Частота ν связана с длиной волны λ света соотношением ν = c / λ, где с-скорость света.
Строение атомов. Атом имеет положительно заряженное ядро, вокруг которого находятся отрицательно заряженные электроны. По представления классической физики электроны вращаются вокруг ядра по определенным траекториям - орбитам. Согласно представлениям квантовой механики электроны находятся вокруг ядра внутри электронного облака, границы которого размыты. Можно говорить лишь о той или иной вероятности обнаружения электрона внутри этого электронного облака. Электронное облако, внутри которого находится электрон, часто называют орбиталью. (Не путать с орбитой!). Электроны многоэлектронного атома находится на орбиталях, которые могут различаться размерами и формой. Орбитали могут иметь форму сферы, гантелей, лепестков и т. д. Если атом находится в основном состоянии, то орбитали внешних электронов имеют минимальные размеры. Если к атому подвести энергию, то размеры орбиталей внешних электронов будут увеличиваться, может изменяться также и их форма. Говорят, что атом при этом переходит в возбуждённое состояние с более высоким значением энергии валентных электронов.
Поскольку раскалённые одноатомные газы и пары излучают линейчатые спектры, рассмотрим процесс испускания света на примере самого простого атома - атома водорода, в электронной оболочке которого находится всего один электрон.
Согласно представлениям квантовой механики энергия этого электрона может изменяться только дискретно и определяется значением главного квантового числа n, которое одновременно определяет и размер электронного облака (орбитали). Если n = 1, электрон находится в основном состоянии, то есть находится на наименьшей по размеру орбитали и, следовательно, имеет самое низкое значение энергии -Е1 (Необходимо отметить, что энергия электрона имеет здесь отрицательное значение, так как за нулевое значение принимают энергию ионизации атома водорода, т.е. энергию, необходимую для отрыва электрона от атома). В основном состоянии электрон может находиться сколько угодно долго.
Если к атому водорода подвести энергию, например, нагреть, то электрон переходит в возбужденное состояние, то есть переходит на более высокие орбитали, где его энергия больше. Согласно квантовым представлениям энергия электрона может иметь при этом только ряд дискретных значений:
-En = -E1/n2
где n = 1, 2, 3 …- главное квантовое число. Через время порядка 10-8 с электрон переходит на более низкие орбитали, то есть в состояние с меньшей энергией. В процессе такого перехода электрон излучает фотон, который и уносит излишек энергии электрона. Обозначим буквой k главное квантовое число орбитали, с которой ушёл электрон, а буквой n - главное квантовое число орбитали, на которую пришёл электрон. Тогда энергия фотона в соответствие с законом сохранения энергии ЕФ = -Еk - (-Еn). Здесь Еk -энергия электрона на орбитали, с которой ушёл электрон, а Еn -энергия электрона на орбитали, на которую электрон пришёл. Длину волны λ излучённого фотона можно найти из уравнения:
hν = hc/λ = - Еk - (-Еn) =-E1(1/k2 -1/n2) = E1(1/n2 - 1/k2).
Здесь k- главное квантовое число орбитали, с которой ушёл электрон, n- главное квантовое число орбитали, на которую электрон пришёл. При каждом таком переходе электрона излучается фотон с длиной волны λ, и в спектре испускания будет видна одна цветная линия. Если энергия, подведённая к водороду, будет достаточно велика (достаточно высокая температура нагрева), то будут возбуждены энергетические уровни с большими значениями главного квантового числа n. Следовательно, может быть совершено большее количество переходов электрона на более низкие энергетические уровни, сопровождающиеся испусканием фотонов с различными дискретными значениями λ. На спектре испускания при этом будет наблюдаться дополнительное количество линий.
На рис. 1 горизонтальными линиями представлены энергетические уровни основного и возбуждённых состояний атома водорода. Стрелками указаны возможные переходы электрона, при которых происходит излучение фотонов.
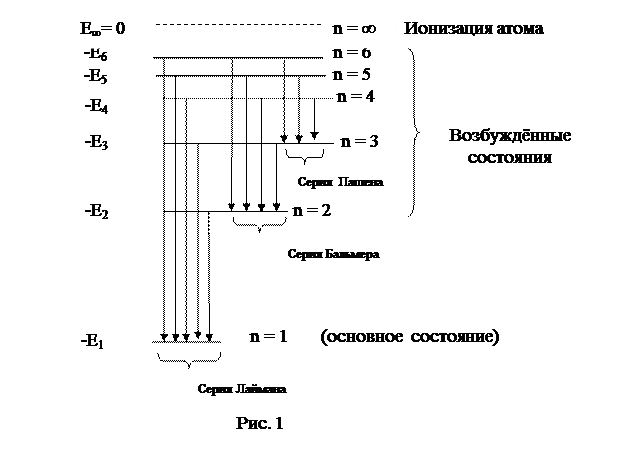 В спектре излучения атома водорода при этом будет наблюдаться несколько серий линий. При переходе электронов из возбуждённых состояний в состояние с n = 1, излучается серия линий в ультрафиолетовой области (серия Лаймана);
В спектре излучения атома водорода при этом будет наблюдаться несколько серий линий. При переходе электронов из возбуждённых состояний в состояние с n = 1, излучается серия линий в ультрафиолетовой области (серия Лаймана);
 при переходе электронов в состояние с n = 2 - серия линий в видимой области (серия Бальмера); при переходе электронов в состояние с n = 3 - серия линий в инфракрас
при переходе электронов в состояние с n = 2 - серия линий в видимой области (серия Бальмера); при переходе электронов в состояние с n = 3 - серия линий в инфракрас  ной области (серия Пашена).
ной области (серия Пашена).
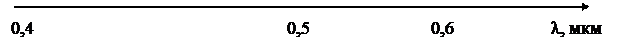 |
 |
|
 На рис. 1 а приведён спектр испускания атома водорода в видимой области.
На рис. 1 а приведён спектр испускания атома водорода в видимой области.
В многоэлектронных атомах дискретные значения энергии возбужденных электронов определяется не только главным квантовым числом n, но и квантовыми числами ℓ, m и s. Орбитальное квантовое число ℓ = 0, 1, 2,……(n -1) характеризует форму электронного облака. Магнитное квантовое число m = 0, ±1, ±2, …..±ℓ, характеризует ориентацию электронного облака в пространстве относительно направления магнитного поля. Спиновое квантовое число s = ±½ характеризует ориентацию собственного момента импульса (спина) электрона в пространстве относительно направления магнитного поля.
Следствием этого обстоятельства является наличие у многоэлектронных атомов большого количества энергетических уровней и возможных переходов с них возбуждённых электронов с испусканием фотонов, а, значит и большого количества линий в спектрах испускания. В данной работе имеется возможность наблюдения спектра испускания в видимой области паров атома ртути, на внешней оболочке которой находится два электрона, и одноатомного газа неона, во внешней оболочке которого находится 8 электронов.
В разреженном газе или паре атомы находятся на больших расстояниях друг от друга, являются независимыми излучателями и дают линейчатые спектры испускания. Атомы в молекулах расположены близко друг к другу, происходит взаимодействие их электрических и магнитных полей. Из-за взаимодействия энергетические уровни атомов испытывают дополнительные расщепления, а спектры испускания становятся "полосатыми", состоящими из большого количества линий.
На атом, находящийся в кристаллической решётке твёрдого тела, оказывают влияние все другие атомы решётки таким образом, что каждый энергетический уровень отдельного атома разбивается на подуровни, количество которых равно количеству атомов в твёрдом теле. Громадное количество энергетических уровней, с которых могут переходить возбуждённые электроны, обуславливает сплошной спектр излучения раскалённых твёрдых тел и жидкостей.
 2015-05-14
2015-05-14 5348
5348