Любые газы при достаточном разрежении и не очень низких температурах удовлетворяют следующим условиям:
- соударения молекул происходят практически абсолютно упруго;
- размерами молекул можно пренебречь по сравнению с межмолекулярными расстояниями, поэтому силы притяжения между ними не проявляются.
Такие газы принято считать идеальными.
Внутренней энергией системы называется энергия этой системы за вычетом кинетической энергии движения системы как целого и ее потенциальной энергии во внешнем поле сил. Следовательно, в понятие внутренней энергии включается кинетическая энергия молекул, потенциальная энергия взаимодействия между молекулами и атомами. По определению, молекулы идеального газа не взаимодействуют между собой, поэтому во внутреннюю энергию идеального газа потенциальная энергия вклада не дает, а учитывать следует только кинетическую энергию отдельных молекул.
Внутренняя энергия одного моля идеального газа равна произведению числа молекул на среднюю энергию одной молекулы 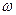 :
:
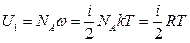 , (2)
, (2)
где 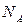 = 6,02
= 6,02  10 23 моль -1 - число Авогадро (количество молекул в одном моле);
10 23 моль -1 - число Авогадро (количество молекул в одном моле);
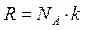 ,
,
где R - универсальная газовая постоянная.
Внутренняя энергия произвольного количества вещества 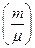 идеального газа:
идеального газа:
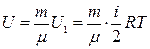 , (3)
, (3)
где m - масса газа,
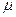 - молярная масса.
- молярная масса.
 2015-05-14
2015-05-14 1551
1551
