Атомы, ядра которых имеют конкретные значения А и Z, называются нуклидами. Для обозначения нуклида используют две формы записи: (А,Z) или 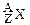 , где Х - символ химического элемента, атомы которого имеют соответствующее ядро. Например, (12,6) или
, где Х - символ химического элемента, атомы которого имеют соответствующее ядро. Например, (12,6) или 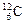 - соответствующий нуклид углерода. Поскольку символ химического элемента однозначно связан с Z, то часто атомный номер в форме записи с указанием символа химического элемента опускают и пишут просто
- соответствующий нуклид углерода. Поскольку символ химического элемента однозначно связан с Z, то часто атомный номер в форме записи с указанием символа химического элемента опускают и пишут просто 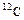 . Такие же обозначения используются и для ядер.
. Такие же обозначения используются и для ядер.
Атомы, ядра которых имеют в своем составе одинаковое число протонов Z, но различающиеся числом нуклонов А, называются изотопами химического элемента. Вещества, имеющие в своем составе атомы изотопов, имеют одинаковые химические свойства, но различную плотность, температуру плавления, кипения и пр., т.е. различаются физическими свойствами. Например: 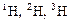 изотопы водорода. 1Н - протий (легкий водород); 1Н - дейтерий (тяжелый водород, употребляют также символ
изотопы водорода. 1Н - протий (легкий водород); 1Н - дейтерий (тяжелый водород, употребляют также символ 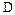 , для ядра - d); 3Н - тритий (сверхтяжелый водород, употребляют также символ
, для ядра - d); 3Н - тритий (сверхтяжелый водород, употребляют также символ 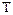 , для ядра d). 233U, 235U, 238U - изотопы урана. Однако об изотопе имеет смысл говорить, подразумевая его принадлежность к химическому элементу. Поэтому 235U- делящийся нуклид урана, а не делящийся изотоп урана. Таким же образом 3Н - радиоактивный нуклид водорода, а не радиоактивный изотоп, так как и в этом случае подразумеваются физические характеристики ядра, а не соответствующие химические свойства атома.
, для ядра d). 233U, 235U, 238U - изотопы урана. Однако об изотопе имеет смысл говорить, подразумевая его принадлежность к химическому элементу. Поэтому 235U- делящийся нуклид урана, а не делящийся изотоп урана. Таким же образом 3Н - радиоактивный нуклид водорода, а не радиоактивный изотоп, так как и в этом случае подразумеваются физические характеристики ядра, а не соответствующие химические свойства атома.
Нуклиды, ядра которых имеют одинаковое число нуклонов (одинаковое массовое число А), но различное число протонов Z, называют изобарами. Например: 3Н и 3Не - изобары трития и гелия, 10Ве, 10В, 10С - изобары бериллия, бора и углерода.
Нуклиды с одинаковым числом нейтронов в составе ядра называют изотонами. Например, 2Н и 3Не - изотоны водорода и гелия.
 2015-05-18
2015-05-18 788
788








