1. По известным молекулярным массам компонентов µ1 и µ2 рассчитать газовые постоянные 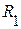 и
и 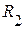 (по формуле
(по формуле 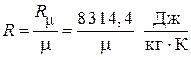 ) и удельные массовые теплоёмкости
) и удельные массовые теплоёмкости 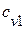 ,
, 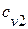 ,
, 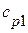 ,
, 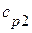 (по классической теории теплоёмкостей, приложение 1),
(по классической теории теплоёмкостей, приложение 1), 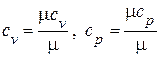 .
.
2. По заданным массам газов рассчитать массовые доли компонентов смеси,
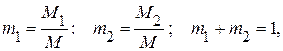
где 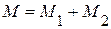 – полная масса смеси,
– полная масса смеси,
удельные теплоёмкости смеси
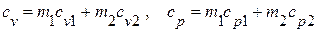 ,
,
газовую постоянную смеси
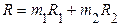
и показатель адиабаты смеси 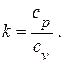
3. По уравнению состояния 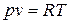 и соотношениям между параметрами в политропном процессе,
и соотношениям между параметрами в политропном процессе,
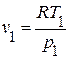 ,
, 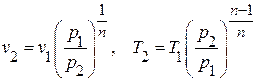 ,
,
определить недостающие параметры. Все параметры в начале и конце процесса занести в табл.2.
Таблица 2
Термодинамические параметры в начальном и конечном состояниях
| Параметры | Размерность | Состояние 1 | Состояние 2 |
| p | бар | ||
| v | м3/ кг | ||
| t | ºC | ||
| T | K |
4. Рассчитать удельные характеристики процесса:
удельную работу изменения объёма,
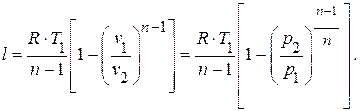
удельную внешнюю работу,
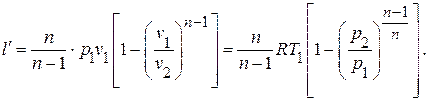
(после этого можно проверить правильность расчетов, определив величину показателя политропы как 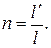 )
)
удельное количество теплоты процесса,
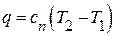 ,
,
для чего необходимо предварительно вычислить удельную массовую теплоёмкость 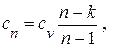
изменение удельных величин термодинамических функций
– внутренней энергии 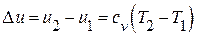 ,
,
– энтальпии 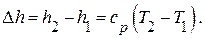
– энтропии 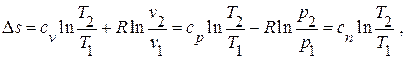
Для нахождения полных характеристик процесса удельные необходимо умножить на массу смеси. Полученные величины занести в табл. 3.
Таблица 3
Результаты расчета политропного процесса
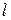
| кДж/ кг | 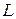
| кДж | |||
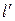
| кДж/ кг | 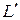
| кДж | |||
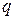
| кДж/ кг | 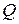
| кДж | |||
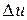
| кДж/ кг | 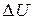
| кДж | |||
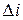
| кДж/ кг | 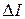
| кДж | |||
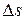
| кДж/(кг·К) | 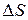
| кДж/К |
5. Результаты расчетов проверить по первому закону термодинамики:
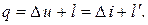
Относительная ошибка расчёта может быть оценена из сравнения количеств теплоты процесса, полученных двумя способами. Погрешность не должна превышать 5%.
6. Изобразить процесс в масштабе на диаграммах 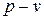 и
и 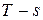 .
.
 2015-05-20
2015-05-20 208
208








