Данным методом можно определением рН растворов в присутствии окислителей, восстановителей, каталитических ядов, многих солей. Он особенно удобен в промышленных системах автоматического контроля и регулирования кислотности среды.
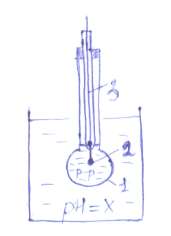
Устройство стеклянного электрода:
1 — тонкостенный шарик из специального сорта стекла, наполненного буферным раствором или раствором НСl концентрации 0,1н.
2 — платиновая проволока, впалнная во внутреннюю трубу, электролитически покрытая сначала слоем серебра, а затем хлорида серебра; обеспечивает контакт с внутренним буферным раствором, содержанием хлорид-ионы; 3- медная проволока, обеспечивающая контакт с внешней цепью. Стеклянный электрод опущен в раствор с неизвестным значением рН.
Потенциал стеклянного электрода в отличие, например, от водородного и хингидронного электродов включает скачки: 1 — на границе раздела стекло—исследуемый раствор; 2 — на границе раздела стекло-буферный раствор; 3 — на границе раздела буферный раствор-металл внутреннего электрода.
Катионы щелочных металлов, входящие в состав стекла, хотя и в незначительной мере, но участвуют в обмене с ионами водорода раствора (константа обменного равновесия равна 10-10-10-14).
Однако этого вполне достаточно, чтобы между стеклом и раствором возник скачок потенциала 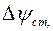 величина которого зависит от рН раствора:
величина которого зависит от рН раствора:
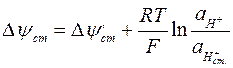 ;
;
где 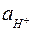 и
и 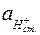 — активности ионов водорода в растворе и в стекле;
— активности ионов водорода в растворе и в стекле; 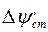 — постоянное для данного сорта стекла слагаемое скачка потенциала. Если выразить
— постоянное для данного сорта стекла слагаемое скачка потенциала. Если выразить 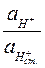 через константу обмена и учесть при этом, что в кислой среде
через константу обмена и учесть при этом, что в кислой среде 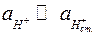 (
(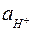 — активность ионов щелочного металла в растворе), то
— активность ионов щелочного металла в растворе), то 
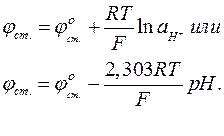
Это уравнение справлены при 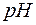 < 10 — 12.
< 10 — 12.
Потенциал стеклянного электрода определяется измерением ЭДС цепи, состоящей из внешнего электрода сравнения, например, каломельного или стеклянного:
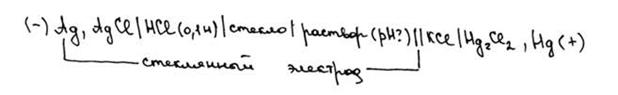
ЭДС этой цепи 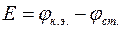 или
или 
Постоянная стеклянного электрода 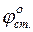 включает постоянные скачки потенциалов стекло-исследуемый раствор, стекло-стандартный (буферный) раствор и скачок потенциала внутреннего электрода.
включает постоянные скачки потенциалов стекло-исследуемый раствор, стекло-стандартный (буферный) раствор и скачок потенциала внутреннего электрода. 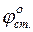 определяется путем калибровки стеклянного электрода по буферным раствором. При известной величине
определяется путем калибровки стеклянного электрода по буферным раствором. При известной величине 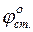 может быть вычислен рН:
может быть вычислен рН:
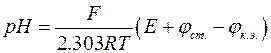 .
.
 2015-05-10
2015-05-10 4489
4489








