Опыт №8
Cu(OH)2 + 2NaOH = Na2[Cu(OH)4] - тетрагидроксокупрат натрия
Cu(OH)2+ H2SO4= [Cu(H2O)4]SO4 сульфат тетра-аквамеди(II)
Na2[Cu(OH)4]: [Cu(OH)4]2- - внутренняя сфера, 2Na+ - внешняя сфера, Cu2+ - комплексообразователь, (OH)4 - лиганды.
[Cu(H2O)4]SO4: [Cu(H2O)4]2+ - внутренняя сфера, Cu2+ - комплексообразователь, H2O – лиганды, SO42- - внешняя сфера.
[Cu(OH)4]2-↔ Cu2++4OH –
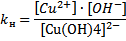
[Cu(H2O)4]2+↔ Cu2++4H2O
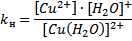
Опыт №9
Cu(OH)2+NH4OH → [Cu(NH3)4](OH)2 – гидроксид тетра аммин меди(II)
Cu(OH)2+NH4+=[Cu(NH3)4]2+
[Cu(NH3)4](OH)2 : [Cu(NH3)4]2+ - внутренняя сфера, Cu2+ - комплексообразователь, NH3 – лиганды, OH- - внешняя сфера.
Cu2+: 1s22s22p63s23p63d5, четыре атомные орбитали, sp3 гибридизация, вид тетраэдра.
NH3 – лиганд, который может изменить свои свойства. Происходит смещение электронной плотности к положительному заряду.
Опыт №10 (а)
CoCl2+2HCl=H2[CoCl4] – раствор синий
CoCl2+6H2O = [Co(H2O)6]Cl2
Опыт №10 (в)
CoCl2+ NH2CNS→(NH3)2[Co(CNS)4] +2NH4Cl
CoCl2+6H2O = [Co(H2O)6]Cl2
[Co(H2O)6]Cl2+4 NH4CNS → (NH4)2+[Co(CNS)4]+NH4Cl+6H2O
Раствор стал синим из-за образования ионов [(Сo(CNS)4]2-
Опыт №11 (а)
NH4[Co(CNS)4]+ 6H2O ↔ [Co(H2O)6]Cl2+4NH4CNS
[Co(H2O)6]2-↔ Co2++4CNS
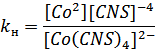
При добавлении воды равновесие смещается в сторону образования ионов Co2+ и CNS из внутренней сферы, то есть изменение 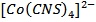 увеличивается.
увеличивается.
Опыт №13
H2O2+2NaOH+ 2K3[Fe(CN)6]→O2↑ + 2H2O + 3K2[Fe(CN)6]
 Fe3++e→Fe2+ 2
Fe3++e→Fe2+ 2
H2O2+2OH-→ O2↑ + 2H2O+2e 1
Выводы
Были решены задачи и проведены опыты по изучению комплексных соединений. Элементы могут образовывать разные комплексы. В зависимости от комплексов растворы могут иметь различный цвет. Комплексы, образованные одним элементом, могут различаться, и при этом степень окисления этого элемента может оставаться неизменной. Также Комплексные соединения могут участвовать окислительно-восстановительных реакциях.
 2015-05-10
2015-05-10 3754
3754








