ЭЛЕМЕНТЫ ЗОННОЙ ТЕОРИИ ТВЕРДЫХ ТЕЛ.
Отличительной особенностью микросистем (атомов, молекул, ионов) является то, что среди бесконечного множества состояний, в которых они могут находиться, наблюдаются такие состояния, между которыми невозможны непрерывные переходы. Переходы осуществляются не через множество промежуточных состояний, а "скачкообразно". При таких переходах характеристики состояний (энергия, импульс, механический и магнитный моменты и др.) изменяются скачкообразно, т.е. имеют ряд дискретных значений − квантуются. Целые или полуцелые числа, определяющие значения квантующихся величин, называются квантовыми числами.
Для характеристики состояния микрочастицы в атоме введены четыре квантовых числа: три (n,l,m - главное, орбитальное и магнитное) соответствуют степеням свободы микрочастицы при ее перемещении в пространстве, четвертое квантовое число (s) не связано с пространственными перемещениями частицы и описывает собственный механический и магнитный моменты, которыми может обладать частица.
Например, полная энергия электрона в атоме водорода, получаемая как результат решения уравнения Шредингера для атома водорода, равна
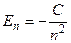 , (1)
, (1)
где С - постоянная величина, n - главное квантовое число, которое может принимать значения 1,2,3...и т.д.
Квантовое число l - характеризует орбитальные механические и магнитные моменты электрона, m - их проекции на фиксированную ось.
Электрон в изолированном атоме может иметь только дискретные значения энергии, называемые энергетическими уровнями (эти значения зависят от строения атома), промежуточные значения энергии запрещены.
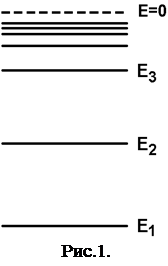 Изолированный атом характеризуется серией энергетических уровней. У каждого элемента имеется характерная для него совокупность уровней − энергетический спектр (рис.1). Заполнение уровней электронами определяется принципом минимума энергии и принципом Паули. При Т= 0 К "заполняются" уровни с наименьшей энергией (принцип минимума энергии). На одном уровне не может находиться более двух электронов с одинаковыми квантовыми числами n,l,m (принцип Паули).
Изолированный атом характеризуется серией энергетических уровней. У каждого элемента имеется характерная для него совокупность уровней − энергетический спектр (рис.1). Заполнение уровней электронами определяется принципом минимума энергии и принципом Паули. При Т= 0 К "заполняются" уровни с наименьшей энергией (принцип минимума энергии). На одном уровне не может находиться более двух электронов с одинаковыми квантовыми числами n,l,m (принцип Паули).
Совокупность уровней атома с распределенными по ним электронами называют электронным состоянием или электронной конфигурацией. Состояния с одинаковыми энергиями называют вырожденными, а число состояний с одинаковыми энергиями называют кратностью вырождения.
 2015-05-13
2015-05-13 930
930







