Второй закон термодинамики определяет направление, в котором протекают процессы, устанавливает условия преобразования тепловой энергии в механическую, а также определяет максимальное значение работы, которая может быть произведена тепловым двигателем.
Математически второй закон термодинамики может быть выражен следующим образом:
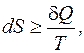 (5.1)
(5.1)
где 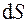 – бесконечно малое приращение энтропии системы;
– бесконечно малое приращение энтропии системы;
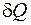 – бесконечно малое количество теплоты, полученное системой от источника теплоты.
– бесконечно малое количество теплоты, полученное системой от источника теплоты.
Знак равенства соответствует обратимым процессам, знак неравенства – необратимым. Чем выше степень необратимости процессов, тем сильнее возрастание энтропии.
Первый и второй законы термодинамики для обратимых процессов могут быть записаны совместно в виде термодинамических тождеств:
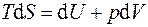 ; (5.2)
; (5.2)
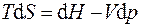 . (5.3)
. (5.3)
Эксергия системы – это максимальная работа, которую может совершить система при переходе в состояние равновесия с окружающей средой. Эксергетический анализ работы теплоэнергетических и технологических установок учитывает не только количественные, но и качественные характеристики энергоресурсов в различных элементах установок, а также необратимость протекающих в них процессов.
Эксергия тепла термодинамического процесса 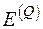 , Дж находится как
, Дж находится как
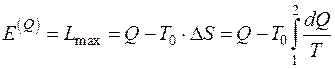 , (5.4)
, (5.4)
где Q – теплота термодинамического процесса, Дж;
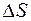 – изменение энтропии рабочего тела, Дж/К;
– изменение энтропии рабочего тела, Дж/К;
Т 0 – температура окружающей среды, К.
Эксергия является экстенсивной функцией состояния, поэтому удельная эксергия тепла 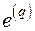 , Дж/К определяется как
, Дж/К определяется как
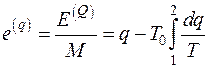 . (5.5)
. (5.5)
Графически удельная эксергия тепла представлена на рис 5.1. Общая площадь под кривой процесса 1–2 соответствует количеству удельной теплоты процесса q. Она состоит из эксергии тепла процесса (площади, заштрихованной вертикальными линиями) и неработоспособной части тепла 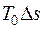 (площади, заштрихованной горизонтальными линиями).
(площади, заштрихованной горизонтальными линиями).
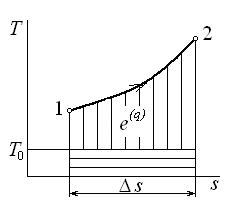
Рис. 5.1. Эксергия тепла термодинамического процесса
Потери работоспособности 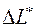 (эксергетические потери) за счет необратимости процессов, протекающих в системе, определяются по формуле Гюи-Стодолы
(эксергетические потери) за счет необратимости процессов, протекающих в системе, определяются по формуле Гюи-Стодолы
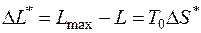 , (5.6)
, (5.6)
где 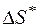 – полное приращение энтропии всех подсистем, входящих в данную систему.
– полное приращение энтропии всех подсистем, входящих в данную систему.
Если в исходном состоянии термодинамическая система имеет параметры U, S, V, а в конечном – находится в равновесии с окружающей средой и имеет параметры 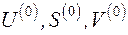 , то эксергия неподвижной термодинамической системы E определяется как
, то эксергия неподвижной термодинамической системы E определяется как
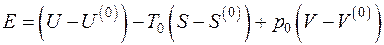 , (5.7)
, (5.7)
а удельная эксергия e неподвижной системы как
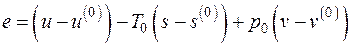 , (5.8)
, (5.8)
где 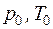 – параметры окружающей среды.
– параметры окружающей среды.
Для неподвижной системы, совершающей некоторый обратимый процесс 1–2, максимальная работа равна убыли эксергии:
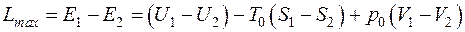 . (5.9)
. (5.9)
Тогда для необратимого процесса уравнение баланса эксергии примет вид
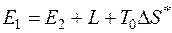 , (5.10)
, (5.10)
то есть при переходе из состояния 1 в состояние 2 эксергия системы расходуется на совершение работы L, а часть работоспособности теряется из-за необратимости процессов.
При нахождении эксергии потока вещества в форме Лагранжа система координат движется вместе с потоком. Если начальные параметры потока H, S, а конечные соответствуют состоянию равновесия потока с окружающей средой 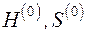 , то выражение для эксергии потока в форме Лагранжа
, то выражение для эксергии потока в форме Лагранжа 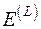 имеет вид
имеет вид
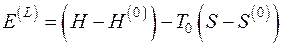 , (5.11)
, (5.11)
а для удельной эксергии потока 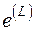 :
:
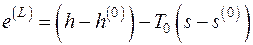 . (5.12)
. (5.12)
Максимальная внешняя работа совершается за счет убыли эксергии потока
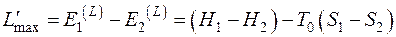 . (5.13)
. (5.13)
Эксергетические потери находятся также по формуле Гюи-Стодолы
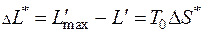 , (5.14)
, (5.14)
тогда уравнение баланса эксергии потока имеет вид
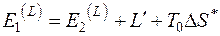 . (5.15)
. (5.15)
Задачи
5.1. Вычислить эксергию тепла изобарного процесса нагрева воздуха от температуры 20 оС до температуры 900 оС, если теплоемкость воздуха ср = 1 кДж/кг, а температура окружающей среды 15 оС.
 2015-05-13
2015-05-13 5153
5153








