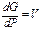 , T=const
, T=const
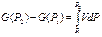 (10)
(10)
Для твердых веществ и жидкостей при умеренных давлениях объем приблизительно постоянен и не зависит от давления; тогда после интегрирования получим
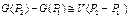 (11)
(11)
Для газа следует использовать уравнение состояния в приближении идеального газа и записать V как функцию от Р. Подставляя уравнение состояния в уравнение (10), получим
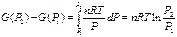 (12)
(12)
Для расчета влияния давления на свободную энергию химической реакции применим уравнения (11) и (12) к каждому продукту реакции и реагирующему веществу.
Если все продукты и исходные вещества — твердые или жидкие, используем уравнение (11):
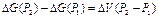 (13)
(13)
где 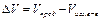
Уравнение (13) показывает, что если объем продуктов реакции больше объема реагирующих веществ (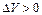 ), то повышение давления будет увеличивать свободную энергию реакции. Если хотя бы одно из реагирующих веществ или продуктов реакции газообразно, можно пренебречь объемом жидкостей и твердых веществ по сравнению с газом и использовать уравнение (12)
), то повышение давления будет увеличивать свободную энергию реакции. Если хотя бы одно из реагирующих веществ или продуктов реакции газообразно, можно пренебречь объемом жидкостей и твердых веществ по сравнению с газом и использовать уравнение (12)
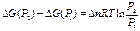
где 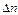 – число моль газообразных продуктов минус число моль газообразных веществ.
– число моль газообразных продуктов минус число моль газообразных веществ.
 2015-05-13
2015-05-13 694
694








