заключаются в изомерии, которая может быть обусловлена также разветвлением углеродного скелета, а также строением своей углеродной цепи.
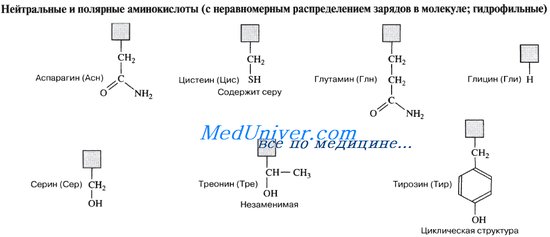
Заряд аминокислоты может изменяться под влиянием среды. Так, при подкислении раствора, с возрастанием концентрации ионов водорода, растет и положительный заряд аминокислоты, отрицательный же соответственно нейтрализуется.
Химические свойства Аминокислоты
Взаимодействие с кислотами. В этом случае происходит протонирование группы СОО- с образованием карбоксильной группы – СООН; анион кислотного остатка присоединяется к группе - H3N+ , полученное соединение относится к классу солей:


 H 3N+ – CH – COO - + HCl Cl- (H 3N+ – CH – COOH)
H 3N+ – CH – COO - + HCl Cl- (H 3N+ – CH – COOH)
R R
Хлористоводородная соль
(гидрохлорид) ά – аминокислоты
Взаимодействие со щелочами. В этом случаегидроксогруппа – ОН- реагирует с группой - H 3N+ , отщепляя от последней протон Н+ с образованием воды (при этом - H 3N+ превращается в аминогруппу - H2N). Полученное соединение также относится к классу солей:


 H 3N – CH – COO - + NaOH H2N – CH – COO- Na+ + H2 O
H 3N – CH – COO - + NaOH H2N – CH – COO- Na+ + H2 O
R R
Натриевая соль ά – аминокислоты
 2015-05-13
2015-05-13 1024
1024








