|
Из кинетической теории газов следует, что молекулярные массы газов пропорциональны их плотностям. Отсюда, зная молекулярную массу одного из газов, например воздуха, и определив экспериментально плотность другого газа, можно найти его молекулярный вес
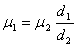 . .
В работе проводится определение молекулярной массы какой-либо легко испаряющейся жидкости. Плотность паров жидкости можно найти, зная предварительно массу, обращаемую затем в пар, и определив объем воздуха, вытесняемого этим паром из некоторого сосуда.
Выполнение работы
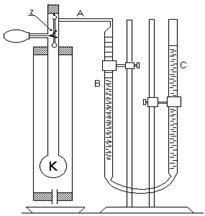
Прибор для определения молекулярных масс веществ состоит из длинногорлой узкой колбы K (см. рис.), в которую помещают в ампуле исследуемое вещество. Колба соединена с бюреткой В при помощи трубки A, по которой воздух, вытесненный парами жидкости, попадает из колбы в бюретку. Бюретка соединена резиновой трубкой с сосудом C, который, как и бюретка, частично заполнен водой.
Взвесив пустую ампулу (с точностью до 0,5 мг), наполняют её исследуемым веществом, запаивают и взвешивают опять. Разность масс дает массу вещества m. Затем нагревают колбу K парами кипящей воды до тех пор, пока воздух, расширяясь, не перестанет из нее выходить, и записывают деление бюретки, против которого стоит уровень воды.
Ампулку подвешивают за крючок, сделанный при запаивании капилляра, к перекладине металлической петли, продетой в пробку, и лопаточкой z переламывают капилляр ампулки. Жидкость в ампулке, испаряясь, вытесняет воздух из K, а последний - воду из В. Опуская сосуд C, поддерживают в колбе атмосферное давление. Когда вода в бюретке перестанет опускаться, замечают снова деление бюретки, против которого устанавливается уровень воды.
Разность отсчетов даст объем воздуха V , вытесненного из К. Этот воздух, попав в бюретку, охладился до комнатной температуры, которую отмечают по термометру. Так как пары жидкости в колбе не насыщают пространства, (это определяется количеством вещества, набранного в ампулу), можно считать, что объемы, занимаемые паром и вытесненным им воздухом, равны, поэтому, будем ли мы в вычислениях пользоваться объемом воздуха или пара, результат получится одинаковый. Так как мы берем плотность воздуха при нормальных условиях, то и найденный объем пара надо привести к тем же условиям
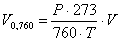 . .
Давление воздуха в бюретке определяют следующим образом. В бюретке над водой полное давление слагается из давления насыщенного пара воды 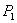 и давления воздуха Р. Сумма этих давлений равна атмосферному, так как уровни воды в В и С одинаковы. Таким образом, обозначив атмосферное давление через Н , имеем: и давления воздуха Р. Сумма этих давлений равна атмосферному, так как уровни воды в В и С одинаковы. Таким образом, обозначив атмосферное давление через Н , имеем:
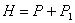 . .
Атмосферное давление измеряют с помощью барометра, а 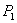 находят из таблиц. находят из таблиц.
Измерив таким образом плотность пара исследуемой жидкости, можно найти её молекулярный вес.
|











