Можно ли приготовить раствор Са(ОН)2 концентрации с =2.10-3 моль/л, если ПР Са(ОН)2 = 6.10-6
Решение. Са(ОН)2 (тв) Û Са 2+(р-р) + 2 ОН -(р-р)
1)Рассчитаем ионную силу раствора:
I = ½(С Ca2+ . z 2Ca2+ + c OH- . z 2OH-) = 8.10-3;
2)По правилу ионной силы определим коэффициенты активности из таблицы: gСа2+≈ 0,61 gОН-≈ 0,93
3)Рассчитаем произведение активностей ПА в растворе требуемой концентрации:
ПА = а Са2+ . (а ОН-)2 = 0,61.2.10-3(0,93.4.10-3)2 = 1,69.10-8
ВЫВОД: ПА < ПРтабл ® раствор заданной концентрации можно приготовить.
Зная ПР, легко рассчитать растворимость с Р и наоборот:
А n B m (тв) Û n A m +(нас.p-р) + m B n -(нас.p-р)
nс Р mс Р моль/л
ПР = 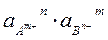 = (gА m+×с Аm+) n × (gB n-× с Bn-) m= (gА m+×n × с Р) n × (gB n-×m ×с Р) m
= (gА m+×с Аm+) n × (gB n-× с Bn-) m= (gА m+×n × с Р) n × (gB n-×m ×с Р) m
=( gА m+)n ×( gB n-)m × nn × mm ×(с Р) n+m, отсюда
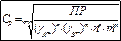 растворимость малорастворимого сильного электролита
растворимость малорастворимого сильного электролита
если g ® 1 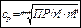 растворимость слабого электролита или сильного с очень малой I
растворимость слабого электролита или сильного с очень малой I
 2015-05-26
2015-05-26 173
173







