При адсорбции газов и паров на поверхности многих адсорбентов образуется полимолекулярный адсорбционный слой. В этих случаях теория Ленгмюра неприменима и для различного рода расчетов пользуются теорией БЭТ.
Теория БЭТ устанавливает следующую зависимость между Г и p:
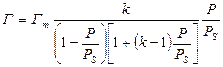
Гm -адсорбционная емкость насыщенного монослоя, определяющаяся размером “посадочной” площадки молекулы газа, т.е. площадью, которую она занимает в насыщенном монослое;
k -константа, зависящая от энергии взаимодействия молекул в адсорбционном слое;
PS -давление насыщенного пара.
Уравнение В Ленгмюра вида:
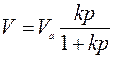
Va – адсорбционный объем,
V – равновесный объем адсорбата.
k- константа, пропорциональная энергии взаимодействия молекул газа с адсорбентом.
р – давление (равновесное)
можно привести к виду:


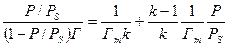
В таком виде уравнение БЭТ является уравнением прямой линии, если функцией считать величину, стоящую слева, а аргументом — P/PS.
Теория БЭТ используется для расчета удельной поверхности адсорбентов (поверхности единицы массы адсорбента) по экспериментально полученной изотерме адсорбции.
Для определения удельной поверхности адсорбента S строят график зависимости P/PS/(1- P/PS)Г от P/PS.
По угловому коэффициенту прямой, равному, (k-1)/kГm, и, величине отрезка, отсекаемого на оси ординат при P/PS =0 и равного 1/Гmk, рассчитывают Гm.
Удельная поверхность вычисляется по формуле:
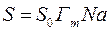
S0 -площадь, занимаемая одной молекулой газа в адсорбционном слое;
Na -постоянная Авогадро.
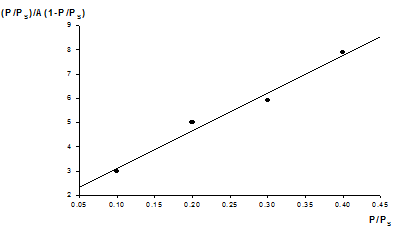
Изотерма адсорбции в координатах линейной формы уравнения БЭТ.
Для адсорбции из растворов линейная форма уравнения БЭТ выглядит таким образом:
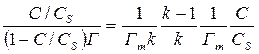
Сs-концентрация насыщенного раствора.
Изотерму адсорбции строят так же, как и в первом случае, в координатах соответствующих этому уравнению. Аналогично вычисляется удельная поверхность:
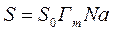
 2015-06-14
2015-06-14 1441
1441
