Решение
Mr(Me2CO3.10H2O) = 240 + 2x
0,7273 = 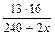 ; 240 + 2x =
; 240 + 2x = 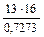 ; x = 23 Þ Nа
; x = 23 Þ Nа
Na2CO3.10H2O
Na2CO3.10H2O ¾¾®Na2CO3
1 моль 1 моль
286 г/моль 106 г/моль n(Na2CO3) = 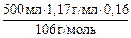 = 0,883 моль
= 0,883 моль
m(Na2CO3.10H2O) = 0,883 моль × 286 г/моль = 252,54 г
m(H2O) = 500 мл × 1,17 г/мл - 252,54 г = 332,4 г
II способ
w%(Na2CO3 в кристаллогидрате) = 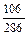 × 100% = 37,063%
× 100% = 37,063%
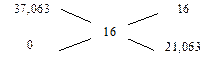
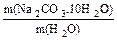 =
= 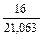 m(16%-ного раствора) = 500 мл × 1,17 г/мл = 585 г
m(16%-ного раствора) = 500 мл × 1,17 г/мл = 585 г
m(Na2CO3.10H2O) = 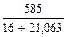 ×16 = 252,54 г. m(H2O) =
×16 = 252,54 г. m(H2O) = 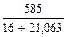 ×21,063 = 332,46 г.
×21,063 = 332,46 г.
Решите: Массовая доля металла в соединении MeSO4.7H2O равна 22,648 %. Установите формулу кристаллогидрата. Сколько по массе воды и кристаллогидрата необходимо для приготовления 300 мл 25%-го раствора MeSO4 (с = 1,304 г/мл).
2 К 104,61 мл 20%-го раствора сульфата алюминия (с = 1,226 г/мл) прибавили 117 г 15%-го раствора сульфида щелочного металла. После отделения осадка и газа получился 14,143%-ный раствор сульфата щелочного металла. Определите металл.
 2015-06-14
2015-06-14 431
431







