Осмотическое давление 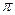 достаточно разбавленных коллоидных растворов может быть найдено по уравнению:
достаточно разбавленных коллоидных растворов может быть найдено по уравнению:
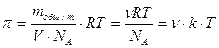 , (9.7)
, (9.7)
где mобщ – масса растворенного вещества; m — масса одной частицы; V – объем системы; NA – число Авогадро; Т – абсолютная температура; v – частичная концентрация; k – постоянная Больцмана.
Это уравнение аналогично известному уравнению Вант – Гоффа для осмотического давления истинных растворов:
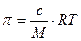
где М – масса одного моля растворенного вещества; с – массовая концентрация.
Молекулярно-кинетические уравнения, справедливые для истинных растворов, применимы и к коллоидным растворам с той лишь разницей, что масса 1 моля вещетва заменяется массой одной частицы. При одной и той же массовой концентрации число частиц (частичная концентрация) в коллоидном растворе значительно меньше, чем в истинном.
Поэтому осмотическое давление лиофобных золей значительно меньше по сравнению с истинными растворами. Весьма малое осмотическое давление лиозолей было причиной ошибки Томаса Грэма, не располагавшего чувствительными осмометрами и считавшего, что у коллоидных растворов осмотическое давление отсутствует.
 2015-06-05
2015-06-05 643
643








