Полиэлектролитами называются ВМС, способные в растворе диссоциировать с образованием высокомолекулярного иона.
В зависимости от природы содержащихся в полимере групп полиэлектролиты можно разделить на три вида:
1) полиэлектролиты, содержащие кислотную группу, например, – СОО 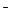 или – ОSО3
или – ОSО3 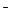 ;
;
2) полиэлектролиты, содержащие основную группу, например – NH3+. Такие вещества в природе не встречаются, но могут быть синтезированы;
3) полиэлектролиты, содержащие одновременно как кислотную, так и основную группы (полиамфолиты). Сюда относятся белки, содержащие группы – СОO 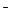 и – NН3+.
и – NН3+.
Все высокомолекулярные электролиты растворяются в полярных растворителях.
Важнейшими представителями полиэлектролитов являются белки. Молекулы белков построены на основе аминокислот и содержат основные группы – HONH3 и кислотные группы – СООН:
HONH3 – R – COOH, где R – достаточно длинный углеводородный радикал.
Следует отметить, что ионогенные группы могут располагаться не только на концах макромолекулы, но и в виде коротких боковых цепей, распределенных по всей длине макромолекулы.
В кислой среде (НС1) подавлена ионизация карбоксильных групп, белок ведет себя как слабое основание:
 HONH3 – R – COOH + Н+ +NH3 – R – COOH + Н2О.
HONH3 – R – COOH + Н+ +NH3 – R – COOH + Н2О.
Молекула приобретает положительный заряд. Так как между одноименно заряженными группами, разбросанными по всей длине молекулы, действуют силы отталкивания, цепная молекула белка в кислой среде будет стремиться развернуться.
Однако при большом избытке НС1 из – за наличия большого количества хлорид – ионов степень ионизации соединения C1NH3 – R – COOH будет понижаться и молекула снова свернется в более плотный клубок.
В щелочной среде (NaOH) из – за большого количества гидроксид – ионов, ионизация групп HONH3+ – подавлена и белок ведет себя как слабая кислота:
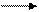 HONH3 – R – COOH+ОН
HONH3 – R – COOH+ОН 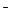 HONH3 – R – COO
HONH3 – R – COO 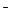 +Н2О,
+Н2О,
приобретая отрицательный заряд. И в этом случае цепная молекула стремится развернуться вследствие электростатического отталкивания групп СОО 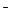 .
.
При большом избытке щелочи из – за большого количества ионов Na+ заряд будет уменьшаться и молекула будет находиться в форме клубка.
Таким образом, как в кислой, так и в щелочной среде молекулы белка обладают нескомпенсированным зарядом разного знака. Регулируя рН белкового раствора, можно добиться перевода белка в изоэлектрическое состояние.
Изоэлектрическим состоянием белка называется состояние белковой молекулы, при котором ее положительные и отрицательные заряды взаимно скомпенсированы. Молекулу белка в изоэлектрическом состоянии можно считать нейтральной, хотя, а ней имеются ионизированные группы.
Условно молекулу белка в изоэлектрическом состоянии можйо изобразить так: +NH3 – R – COO 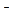
Изоэлектрическая точка белка (ИТБ) – это значение рН, при котором белок переходит в изоэлектрическое состояние.
Так как белок обычно является более сильной кислотой, чем основанием, его ИТБ лежит при рН < 7. Иначе говоря, для достижения изоэлектрического состояния в растворе должен находиться некоторый избыток кислоты, для подавления ионизации кислотных групп. Так как в ИТБ число ионизированных основных и кислотных групп одинаково, гибкая макромолекула сворачивается в клубок.
На форму макромолекул влияет не только рН среды, но и введение в
раствор индифферентного электролита.
Небольшое количество электролита подавляет ионизацию ионогенных групп и приводит к тому, что форма макромолекул приближается к наиболее статистически вероятным конформациям. При больших концентрациях электролитов происходит высаливание вследствие уменьшения растворимости полимера – макромолекулы образуют плотные клубки. Действие ионов на полиэлектролиты изменяется в том порядке, в котором они стоят в лиотропном ряду.
 2015-06-05
2015-06-05 1026
1026








