Для примера рассмотрим водный раствор соли Pb(NO3)2 объемом V = 0,5 л, плотность которого ρ = 1016 кг/м3 = 1016 г/л. Масса растворенного вещества m = 10 г. Необходимо выразить концентрацию раствора в разных вариантах.
Концентрация растворов обозначается: c, или [ ], например с (KCl), или [KCl]. Чаще всего используется второй вариант. Для концентрированных растворов вместо концентрации используется активность раствора (а), где а = γ · с. Величина γ – коэффициент активности – представляет собой поправочный коэффициент, учитывающий взаимодействие частиц реального раствора, приводящее к изменению концентрации. Для разбавленных растворов γ → 1, и вместо активности используется значение концентрации. При выполнении требуемых заданий коэффициент активности не учитывается.
5.1.1. Определим процентную концентрацию раствора. Процентная концентрация (% масс.) показывает, сколько граммов вещества содержится в 100 г раствора. Сначала вычислим массу раствора, содержащегося в 0,5 л:
m р-ра = V · ρ = 0,5 л × 1016 г/л = 508 г.
Если в 508 г раствора содержится 10 г Pb(NO3)2,
то в 100 г раствора содержится х -"- -"- -"-
х = 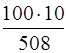 = 1,97,
= 1,97,
т. е. раствор имеет концентрацию равную 1,97 % масс.
5.1.2. Определяем молярную концентрацию раствора. Молярная концентрация (молярность) раствора сМ (моль/л) показывает, какое число молей растворенного вещества содержится в 1 л раствора.
Рассчитаем молярную массу растворенного вещества – Pb(NO3)2:
М (Pb(NO3)2) = 207,2 + 2(14+3·16) = 331,2 г.
Определим число молей Pb(NO3)2, которое содержится в 0,5 л раствора:
1 моль Pb(NO3)2 содержит 331,2 г Pb(NO3)2
х молей Pb(NO3)2 содержит 10 г Pb(NO3)2
х = 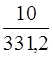 = 0,0302 моля.
= 0,0302 моля.
Затем выясним, сколько молей соли находится в 1 л раствора, если известно, что в 0,5 л содержится 0,0302 моля Pb(NO3)2.
0,5 л раствора содержит 0,0302 моля
1 л раствора содержит х моль
х = 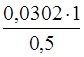 = 0,0604 моля.
= 0,0604 моля.
Таким образом, молярность раствора с М равна 0,0604 моль/л.
5.1.3. Определяем нормальность раствора (молярную концентрацию эквивалента).
Молярная концентрация эквивалента, с экв. или нормальность, н, (моль-экв./л) показывает, какое число молярных масс эквивалента растворенного вещества содержится в 1 л раствора.
Сначала рассчитаем молярную массу эквивалента Mэкв. Pb(NO3)2. Она определяется как отношение молярной массы соли к произведению числа ионов металла на его валентность.
Mэкв. (Pb(NO3)2) = 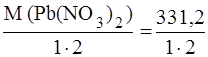 = 165,6 г.
= 165,6 г.
Затем находим молярную концентрацию эквивалента (нормальность) раствора:
так как в 0,5 л раствора содержится 10 г Pb(NO3)2,
то в 1 л раствора содержится х г Pb(NO3)2
х = 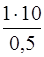 = 20 г.
= 20 г.
В этой массе число молярных эквивалентов составляет:
с экв. = 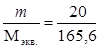 = 0,121 моль-экв.
= 0,121 моль-экв.
Таким образом, молярная концентрация эквивалента (нормальность) раствора Pb(NO3)2 с экв составляет 0,121 моль-экв.
5.1.4. Определяем моляльность раствора.
Моляльность раствора сm (моль/кг) показывает, какое число молей растворенного вещества приходится на 1 кг растворителя (воды).
Сначала рассчитаем массу воды в 0,5 л раствора:
m (Н2О) = m (раствора) - m (Pb(NO3)2) = 508 г - 10 г = 498 г.
Число молей растворенного вещества в 0,5 л, рассчитанное ранее в 5.1.2, составляет 0,0302.
Далее, если в 498 г воды содержится 0,0302 моля Pb(NO3)2,
то в 1000 г воды содержится х моль Pb(NO3)2.
х = 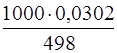 = 0,061 моль/г.
= 0,061 моль/г.
Таким образом моляльность раствора сm составляет 0,061 моль/г.
Задание 5.2. Рассчитайте рН раствора кислоты или щелочи, если известна ее молярная концентрация с М (моль/л) (табл. V.2).
 2015-06-05
2015-06-05 2671
2671








