Внутренняя энергия – кинетическая энергия хаотического движения частиц и энергия их взаимодействия. Она включает в себя энергию электронных оболочек атомов и ионов и внутриядерную энергию.
К внутренней энергии не относится кинетическая энергия движения системы как целого и потенциальная энергия системы во внешнем поле сил.
Фаза – совокупность всех частей т/д системы, обладающих одинаковым химическим составом, находящихся в одинаковом состоянии и ограниченных поверхностями раздела.
Различные вещества, наименьшее количество которых необходимо для образования всех фаз, называются компонентами т/д системы.
Зависимость между числом компонентов (N) и числом фаз определяется правилом Гиббса.
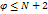
Переход вещества из одной фазы в другую при изменении внешних условий - фазовый переход.
Существует два вида фазовых переходов:
Ф.п. 1 рода сопровождается скачкообразным изменением внутренней энергии и плотности. Связан с выделением или поглощением энергии (плавление и отвердевание).
|
|
|
Ф.п. 2 рода происходит без изменения плотности и внутренней энергии, и осуществляется без выделения или поглощения теплоты. При нём наблюдается изменение теплоёмкости (из пара- в ферромагнетик; в сверхпроводящее состояние; в сверхтекучесть у гелия).
Если система однокомпонентна, то существует три агрегатных состояния. Условия их существования определяются внешними параметрами – давление и температура. Эта зависимость отображается кривой в координатах Р и Т – диаграммой состояний. Она задаёт зависимость между температурой фазового перехода и давлением.

С – сублимация; П – плавление; И – испарение.
Точка, в которой сходятся кривые равновесия, - тройная точка. Каждое вещество имеет только одну тройную точку.
Для двухфазной системы зависимость давления от температуры задаётся уравнением Клапейрона-Клаузиуса.
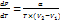
α – скрытая теплота фазового перехода; Т – температура перехода; (V2-V1) – изменение объёма при фазовом переходе
 2015-06-24
2015-06-24 365
365








