В качестве общих рекомендаций по лечению эксперты ЕКО указывают на необходимость оптимизации преднагрузки с помощью внутривенного введения жидкости (если необходимо), рекомендуют применение вазодилататоров (если позволяет уровень АД), короткой инотропной поддержки и ВАБК [ 1 ]. Среди средств инотропной поддержки рассматривают допамин, добутамин, а при их недостаточной эффективности, когда артериальная гипотензия угрожает жизни больного – вазопрессорные препараты (эпинефрин и норэпинефрин). Очевидно, что в этой критической ситуации приходится мириться с возможностью усугубить выраженность гемодинамических нарушений, характерных для кардиогенного шока, и способствовать дальнейшему повреждению миокарда. Для контроля АД при использовании вазопрессорных препаратов предлагают ввести артериальный катетер. В менее тяжелых случаях низкие дозы допамина (до 3 мкг/кг/мин) могут использоваться для улучшения перфузии почек при малом количестве отделяемой мочи. У больных с выраженной артериальной гипоксемией, которую не удается устранить оксигенотерапией, показана поддержка дыхания, вплоть до интубации трахеи с искусственной вентиляцией легких (ИВЛ).
При ИМ эксперты ЕКО рекомендуют использовать допамин в дозе 2,5-5 мкг/кг/мин для улучшения функции почек и рассмотреть целесообразность применения добутамина в дозе 5-10 мкг/кг/мин [2]. Однако представляется, что приведенные дозы могут оказаться слишком низкими для больных с выраженной артериальной гипотензией, если кардиотонические и вазопрессорные препараты – единственный доступный способ поддержки кровообращения. Настоятельно рекомендуется использовать средства механической поддержки кровообращения в качестве временной меры («моста») до хирургического вмешательства. Среди них наиболее доступна ВАБК. Это вмешательство эффективнее, чем известные способы медикаментозного лечения, и лишено многочисленных недостатков, свойственных кардиотоническим и вазопрессорным препаратам (не увеличивает потребность миокарда в кислороде, не способствует его дальнейшему повреждению, не обладает проаритмическим действием). Напротив, оно позволяет увеличить коронарный кровоток в диастолу и снизить работу сердца [1, 15].
Подходы к лечению кардиогенного шока при ИМ, рекомендуемые АКК/ААС, представлены на рисунке 1. При выраженной артериальной гипотензии указывают на необходимость внутривенной инфузии норэпинефрина, при повышенииАД, по крайней мере, до 80мм рт.ст. – осуществить попытку перейти на допамин, а если удастся достигнуть уровня 90 мм рт. ст. – начать вводить добутамин и стремиться уменьшить скорость введения допамина. Для стабилизации гемодинамики у больных, которые быстро не отвечают на медикаментозную терапию и которым может быть проведено инвазивное лечение, рекомендуется использовать ВАБК. Кроме того, предлагают установить плавающий катетер в легочную артерию и осуществлять мониторирование АД через катетер, установленный в лучевую артерию (особенно когда вводятся кардиотонические или вазопрессорные препараты). Эксперты АКК/ААС отмечают, что если реваскуляризация миокарда невозможна, применение различных устройств поддержки кровообращения может быть оправдано в ожидании спонтанного улучшения сократительной способности миокарда (в частности, за счет «оглушенного» миокарда) или до трансплантации сердца [15].
Крайне важным представляется своевременная диагностика выраженных проявлений синдрома низкого сердечного выброса, граничащих с кардиогенным шоком, когда АД поддерживается за счет спазма артериол. Применение у таких больных лекарственных средств, угнетающих сократительную способность миокарда, может спровоцировать появление развернутой картины кардиогенного шока, во многих случаях необратимого. Не исключено, что недостаточный учет этого обстоятельства – одна из причин роста частоты кардиогенного шока в начале применения высокой дозы β-адреноблокатора при достаточно обширном ИМ в крупном контролируемом клиническом испытании COMMIT/CCS2 [19].
Современные представления о наилучших подходах к лечению кардиогенного шока при ИМ как правило основываются на результатах контролируемого клинического исследования SHOCK, проведенного с 1993 по 1998 г. [20, 21, 22]. В нем были изучены 302 больных с ИМ, развившимся в ближайшие 36 часов, у которых проявления кардиогенного шока появились не позднее, чем в предшествующие 12 часов. Больным, рандомизированным в группу ранней реваскуляризации миокарда, чрескожное коронарное вмешательство (ЧKB) или операцию коронарного шунтирования (КШ) рекомендовалось выполнить как можно быстрее, в пределах 6 часов после рандомизации. Больным, вошедшим в группу первоначального медикаментозного лечения, реваскуляризацию миокарда разрешалось осуществлять не ранее, чем через 54 часа после рандомизации. В обеих группах использовались положительные инотропные препараты (99%), и у большинства больных осуществлялась ВАБК (86%). Тромболитическую терапию получили 49% больных в группе раннего инвазивного лечения и 63% больных в группе отсроченных инвазивных вмешательств. Транспортировка в другое лечебное учреждение для инвазивного лечения осуществлялась в 55 % случаев.
В группе раннего инвазивного лечения коронарная ангиография была выполнена в 97 % случаев, реваскуляризация миокарда – и 87% (операция КШ у 37% больных). В группе отсроченного инвазивного лечения коронарную ангиографию выполнили у 67% больных, реваскуляризацию миокарда – у 25%. Выбор метода реваскуляризации зависел от особенностей коронарной анатомии (КШ рекомендовалось выполнять при тяжелом трехсосудистом поражении или стенозе ствола левой коронарной артерии). При таком подходе результаты КШ и ЧKB заметно не различались – через 30 дней смертность составила 45 и 42% соответственно
Хотя через месяц достоверных различий между группами по общей смертности не было (47% в группе раннего инвазивного лечения и 56% при менее агрессивном лечении больных), однако уже через полгода проявилось преимущество раннего инвазивного подхода (общая смертность составляла 50 и 63% соответственно, р=0,03). Иными словами, раннее инвазивное лечение кардиогенного шока при ИМ позволяло предотвратить 130 смертельных исходов на каждую тысячу леченных больных. Это преимущество сохранялось неизменным, как минимум, в ближайшие 6 лет, причем почти две трети больных ИМ с кардиогенным шоком, подвергшихся ранней реваскуляризации миокарда и выписавшихся из стационара, были живы все эти годы. Не было выявлено зависимости эффективности лечения от различных показателей тяжести заболевания и особенностей его лечения (наличие кардиогенного шока при госпитализации или его развитие в последующем, факт перевода в другой стационар для инвазивного лечения, возможность быстро устранить гипоперфузию с помощью внутриаортальной баллонной контрапульсации, вводившийся фибринолитический агент).





 Наиболее вероятная причина
Наиболее вероятная причина
Вмешательства I ряда
| • Жидкость в/в
• Переливание крови (если нужно)
• Воздействие на причину
Рассмотреть вазопрессоры
| | 
|
| Кардиогенный шок с низким сердечным выбросом
| |








 Вмешательства II ряда Вмешательства II ряда
| Норэпинефрин
в/в 0,5 – 30 мкг/кг/мин
| |
|
| САД 70 – 100 мм рт. ст.
Нет признаков шока
| |
| САД < 70 мм рт. ст.
Признаки шока
| |
| САД 70 – 100 мм рт. ст.
Признаки шока
| |
| |
| | | Дальнейшие диагностические / терапевтические мероприятия
• Катетеризация легочной артерии
• Эхокардиография
• Коронарная ангиография при инфаркте / ишемии миокарда
• Дополнительные диагностические исследования
• Внутриаортальная баллонная контрпульсация
• Реперфузионная терапия / реваскуляризация миокарда
| |
Рисунок 1. Неотложное лечение больных инфарктом миокарда с симптомами шока [15, с изменениями]
Результаты отдаленного наблюдения показали, что при раннем инвазивном лечении положительный результат можно распространить и на больных старшей возрастной группы (75 лет и старше).
В группе раннего инвазивного лечения коронарная ангиография была выполнена в 97 % случаев, реваскуляризация миокарда – и 87% (операция КШ у 37% больных). В группе отсроченного инвазивного лечения коронарную ангиографию выполнили у 67% больных, реваскуляризацию миокарда – у 25%. Выбор метода реваскуляризации зависел от особенностей коронарной анатомии (КШ рекомендовалось выполнять при тяжелом трехсосудистом поражении или стенозе ствола левой коронарной артерии). При таком подходе результаты КШ и ЧKB заметно не различались – через 30 дней смертность составила 45 и 42% соответственно
Хотя через месяц достоверных различий между группами по общей смертности не было (47% в группе раннего инвазивного лечения и 56% при менее агрессивном лечении больных), однако уже через полгода проявилось преимущество раннего инвазивного подхода (общая смертность составляла 50 и 63% соответственно, р=0,03). Иными словами, раннее инвазивное лечение кардиогенного шока при ИМ позволяло предотвратить 130 смертельных исходов на каждую тысячу леченных больных. Это преимущество сохранялось неизменным, как минимум, в ближайшие 6 лет, причем почти две трети больных ИМ с кардиогенным шоком, подвергшихся ранней реваскуляризации миокарда и выписавшихся из стационара, были живы все эти годы. Не было выявлено зависимости эффективности лечения от различных показателей тяжести заболевания и особенностей его лечения (наличие кардиогенного шока при госпитализации или его развитие в последующем, факт перевода в другой стационар для инвазивного лечения, возможность быстро устранить гипоперфузию с помощью внутриаортальной баллонной контрапульсации, вводившийся фибринолитический агент). Результаты отдаленного наблюдения показали, что при раннем инвазивном лечении положительный результат можно распространить и на больных старшей возрастной группы (75 лет и старше). Косвенные свидетельства пользы ранней реваскуляризации миокарда у больных этой возрастной категории получены также при анализе регистра больных, не вошедших в исследование SHOCK [23]. Соответственно, у больных ИМ, осложнившимся кардиогенным шоком, ранний инвазивный подход обладал явным преимуществом по влиянию на выживаемость на протяжении длительного времени по сравнению с тактикой, предусматривающей попытки первоначальной медикаментозной стабилизации (даже достаточно агрессивные, с использованием ВАБК). Полученные данные демонстрируют также возможность транспортировки подобных больных в специализированные лечебные учреждения, в которых возможно квалифицированное выполнение реваскуляризации миокарда
Результаты регистра исследования SHOCK предполагают, что наилучшей стратегией лечения кардиогенного шока при ИМ, связанного с нарушенной насосной функцией ЛЖ, является ВАБК со скорейшей реваскуляризацией миокарда [24]. Если инвазивное лечение быстро не доступно, альтернативный подход может заключаться во внутривенном введении фибринолитика и начале ВАБК со скорейшей транспортировкой в соответствующий стационар для реваскуляризации миокарда.
Таким образом, согласно современным представлениям, если причиной кардиогенного шока является острая коронарная недостаточность, наиболее эффективный способ спасения жизни больного – немедленная реваскуляризация миокарда (в зависимости от коронарной анатомии ЧKB или операция КШ). Опираясь на представленные факты, инвазивное вмешательство рекомендуют осуществлять как можно быстрее, однако временной интервал, при котором ожидается польза от инвазивного лечения, достаточно широк – до 36 часов после начала ИМ и 18 часов после появления признаков шока. В случаях, когда нет возможности быстро приступить к процедурам реваскуляризации миокарда (в пределах 90 минут после прибытия бригады скорой медицинской помощи или самостоятельного обращения больного в стационар), у больных с признаками сохраняющейся окклюзии коронарной артерии (стойкими подъемами сегмента ST на ЭКГ) рекомендуют предварительно ввести фибринолитик [2, 15, 25]. Это особенно важно в первые часы заболевания, когда некротизируется максимальный объем жизнеспособного миокарда. В крупных исследованиях GUSTO-I и GUSTO-III y больных с кардиогенным шоком, получивших фибринолитик, смертность в ближайший месяц была наименьшей в случаях, когда использовалась ВАБК и проводилась реваскуляризация миокарда (ЧKB или КШ) [7].
При признаках нестабильности гемодинамики при ОКС без стойких подъемов сегмента ST на ЭКГ эксперты ЕКО и АКК/ААС также рекомендуют неотложную коронарную ангиографию, чтобы в дальнейшем (если будут найдены анатомические показания) безотлагательно выполнить реваскуляризацию миокарда [25-27].





 Наиболее вероятная причина
Наиболее вероятная причина









 Вмешательства II ряда
Вмешательства II ряда

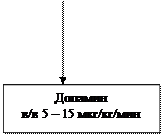

 2015-07-04
2015-07-04 299
299








