
|
Разберём пример с энтальпией. Задача состоит в вычислении изменения энтальпии при увеличении давления, когда нельзя пренебрегать взаимодействием между молекулами. Используя соотношение Н = U + PV и (8.6) получим
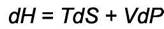
|
(8.7)
На основании (8.7) можно записать две производные:
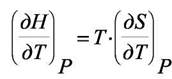
|
(а)
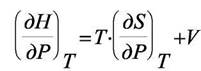
|
(б)
Теперь из (а) и (б) можно найти смешанные производные:
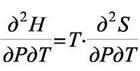
|
(а′)
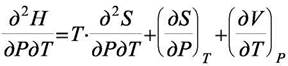
|
(б′)
Так как смешанные производные равны, то из (а′) и (б′) получим
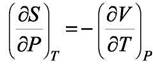
|
(8.8)
Формула (8.8) имеет и самостоятельное значение, так как даёт зависимость энтропии от давления. Подставив (8.8) в (б), получим
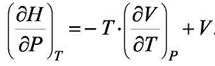
|
(8.9)
Уравнение (8.9) отвечает поставленной задаче. При известном уравнении состояния можно вычислить изменение энтальпии при переходе системы к другому давлению. Например, для идеального газа:
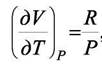
|
Тогда
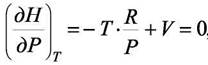
|
 2015-07-04
2015-07-04 377
377








