Впіридиновому кільці можуть проходити реакції електрофільного та нуклеофільного заміщення.
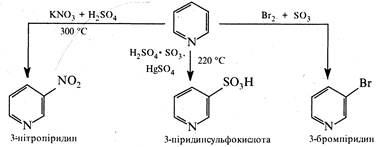
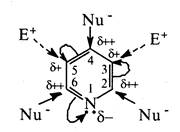 1. Реакції електрофільного заміщення в піридиновому циклі ідуть насилу. Нітрування, сульфування та галогенування піридину відбуваються тільки за жорстких умов. Так, нітрування проходить з низьким віходом при нагріванні піридину з нітратом калію в димлячій сірчаній кислоті; при 300 °С, сульфування відбувається при нагріванні з олеумом (220- 270 °С) в присутності каталізатора сульфату ртуті, бромування можливе при дії брому в олеумі. Електрофільний замісник спрямовується в β-положення циклу:
1. Реакції електрофільного заміщення в піридиновому циклі ідуть насилу. Нітрування, сульфування та галогенування піридину відбуваються тільки за жорстких умов. Так, нітрування проходить з низьким віходом при нагріванні піридину з нітратом калію в димлячій сірчаній кислоті; при 300 °С, сульфування відбувається при нагріванні з олеумом (220- 270 °С) в присутності каталізатора сульфату ртуті, бромування можливе при дії брому в олеумі. Електрофільний замісник спрямовується в β-положення циклу:
Реакції алкілування і ацилювання за Фріделем-Крафтсом для піридину не характерні. Низька реакційна здатність піридинового циклу в реакціях електрофільного заміщення та орієнтація заміщення в β-положення зумовлена електроноакцепторними властивостями атома азоту, котрий, зменшуючи електронну густину на всіх атомах вуглецю циклу, меншою мірою справляє вплив на β-положення, що і визначає місце атаки електрофільним реагентом. Крім того, в реакціях SE з протонними реагентами (нітрування, сульфування) піридин утворює по гетероатому солі піридинію, а з галогенами — донорно-акцепторні комплекси, в яких на атомі азоту з'являється позитивний заряд, а це, в свою чергу, призводить до ще більшої дезактивації піридинового циклу.
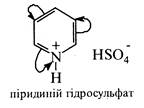
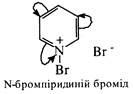
2. Реакції пуклеофільного заміщення через зменшення електронної густини на атомах вуглецю піридинового циклу полегшуються. На відміну від бензолу, піридин досить легко реагує з нуклеофільними реагентами, утворюючи продукти заміщення в положеннях 2, 4 або 6 (α- та β-положення).
З реакцій нуклеофільного заміщення найбільш відоме амінування за Чичибабіним. Воно основане на взаємодії піридину з амідом натрію (NaNH2) при нагріванні. Найкраще проходить амінування у середовищі рідкого аміаку. В результаті реакції утворюється 2-амінопіридин.
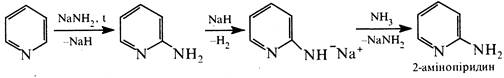
Дальше амінування веде до утворення 2,6-діамінопіридину. Заміщення на аміногрупу атома водню в γ-положенні відбувається тільки в тому разі, як α-положення вже зайняті.
Вперше цю реакцію здійснив у 1914 р. російський хімік-органік О.Є.Чичибабін і тому вона дістала назву реакції Чичибабіна. В дальшому її було розповсюджено на інші гетероциклічні сполуки.
Механізм реакції:
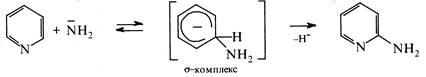
Реакція проходить за механізмом SN2. На першій стадії нуклеофільна частинка NH атакує піридинове кільце з утворенням σ-комплексу. Ha другій стадії σ-комплекс стабілізується шляхом відщеплення гідрид-іона (Н-).
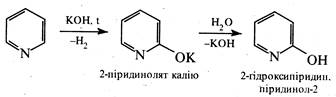
Аналогічно амінуванню відбувається гідроксилування піридинового циклу. При пропусканні парів піридину понад сухим гідроксидом калію при 300-320 °С утворюється 2-гідроксипіридин.
 2015-07-14
2015-07-14 2717
2717








