Пример 1. Рассчитать энергетический эффект химической реакции в стандартных условиях: Al 2 O 3(к) + 3SO 3(г) → Al 2 (SO 4) 3(к). Известны энтальпии образования участвующих в реакции соединений:
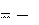 0
0
ΔH298,Al 2 (SO4)3
 0
0
3434 кДж/моль;
ΔH298,Al 2O3
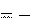
1675 кДж/моль;
395,2 кДж/моль.
Решение. Энтальпия этой реакции рассчитывается по формуле
ΔH0298,p-ции
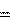 ΔH0298,Al
ΔH0298,Al
2 (SO4)3
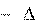 (H0298,Al
(H0298,Al
2O3
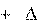
ΔH0298,p-ции
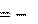 3434
3434
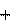 1675
1675
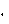
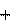 3 395,2
3 395,2
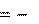 573,4 кДж.
573,4 кДж.
Энтальпия системы в ходе реакции уменьшается, в этом случае энергия выделяется, реакция экзотермическая.
Пример 2. Рассчитать энтальпию реакции
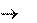 С2Н4(г) + Н2(г) С2Н6(г)
С2Н4(г) + Н2(г) С2Н6(г)
в стандартных условиях, зная энтальпии сгорания участвующих в реакции веществ:
ΔH0
298,сг.С2 Н 4
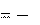 1411,3 кДж/моль;
1411,3 кДж/моль;
ΔH0 ΔH0
298,сг.Н 2
298,сг.С2 Н6
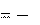 285,5 кДж/моль;
285,5 кДж/моль;
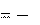 1560,2 кДж/моль.
1560,2 кДж/моль.
Энтальпии реакции можно рассчитать по формулам:
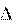
|
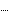 ции
ции
H0298,сг,исх.в-в
H0298,сг.продуктов;
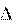
|
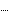 ции
ции
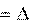
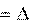
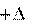
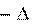
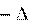
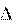 H0298,р
H0298,р
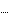 ции
ции
 1411,3
1411,3
 285,5
285,5
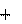 1560,2
1560,2
 136,6 кДж.
136,6 кДж.
Данная реакция экзотермическая.
Пример 3. Определить энтальпию образования метана, зная, что энтальпия реакции горения метана ΔН 0298,р = -804,75 кДж, а стандартные значения энтальпий образования СО 2 и Н 2 О равны соответственно 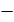 396кДж/моль и –241,8 кДж/моль.
396кДж/моль и –241,8 кДж/моль.
 Решение. СН 4(г) + 2О 2(г) СО 2(г) + 2Н 2 О (г)
Решение. СН 4(г) + 2О 2(г) СО 2(г) + 2Н 2 О (г)
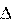 H0298,p
H0298,p
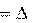
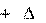 2 H0
2 H0
298,Н2O
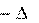
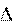
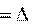
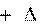
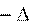 H0298,p
H0298,p 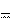
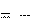 396
396
 2 241,8
2 241,8
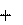 804,75
804,75
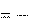 74,85 кДж / моль.
74,85 кДж / моль.
Пример 4. Какое количество тепла выделяется в ходе горения 10 г серы, если стандартное значение энтальпии образования SO 2 равно
-296,9 кДж/моль?
Решение. Уравнение химической реакции горения серы –
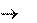 S + O 2 SO 2.
S + O 2 SO 2.
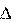 Энтальпия этой реакции определяется по формуле
Энтальпия этой реакции определяется по формуле
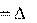
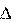 H 0298,p
H 0298,p
реакция экзотермическая.
H 0298,SO 2;
H 0298,p
 296,9 кДж,
296,9 кДж,
Определяем количество тепла, выделенное при горении 10 г серы.
Согласно уравнению реакции 1 моль дает 296,9 кДж тепла. Составляем пропорцию:
32 г S – 296,9 кДж, 10 г S – Х кДж;
Х = 10г ∙ 296,9кДж / 32г = 93кДж.
Пример 5. Вычислить тепловой эффект реакции получения гидроксида кальция из оксида кальция и воды, если стандартная энтальпия образования оксида кальция равна -635,7 кДж/моль, стандартная энтальпия образования воды равна -285,8 кДж/моль, а стандартная энтальпия образования гидроксида кальция равна -986,8 кДж/моль.
Решение.
Уравнение реакции получения негашеной извести из гашеной извести такое:
CaO + H2O = Ca(OH)2.
На основании первого следствия из закона Авогадро:
ΔH0 = ΔH0Ca(OH)2 – (Δ H0CaO + ΔH0H2O) =
–986,8 – (– 635,7 – 285,8) = – 65,3 кДж/моль.
Пример 6. Реакция окисления глюкозы в организме может протекать так:
С6Н12О6 (тв) + 6О2 (г) = 6СО2 (г) + 6Н2О (ж),
D Н = –2803 кДж.
Какое количество теплоты выделится при окислении 800 г глюкозы?
Решение.
М (С6Н12О6) = 180 г/моль.
ν (С6Н12О6) = 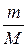 =
= 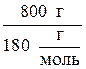 = 4,44 моль.
= 4,44 моль.
Δ H0 = ν (С6Н12О6) · Δ H = 4,44 · (–2803) = – 12458 кДж.
Задания для самоконтроля
1. Составьте термохимическое уравнение реакции разложения карбоната кальция, если при разложении 40 г карбоната кальция поглощается 70,8 кДж теплоты.
Ответ. CaCO3 = CaO + CO2  (г.) – 177 кДж/моль.
(г.) – 177 кДж/моль.
2. Сколько теплоты выделится при полном сгорании 1 м3 смеси, состоящей из 30% (по объему) этилена и 70% ацетилена, если при сгорании 1 моль этих веществ выделяется соответственно 1400 и 1305 кДж?
Ответ. 59 531 кДж.
3. Вычислите теплоту сгорания ацетилена С2Н2, если теплота образования углекислого газа 393,5 кДж/моль, водяного пара – 242 кДж/моль, ацетилена – 226,8 кДж/моль.
Ответ. 1604,4 кДж.
4. По термохимическому уравнению
N2 (г.) + О2 (г.) = 2NО (г.) – 180,7 кДж
вычислите, сколько поглотится теплоты при вступлении в реакцию 5,6 л азота (н. у.).
Ответ. 45,2кДж
5. При сжигании 3 г магния выделилось 75,15 кДж теплоты. Составьте термохимическое уравнение реакции горения магния.
Ответ. 2Mg + O2 = 2MgO + 1202кДж
6. По термохимическому уравнению реакции
2СО (г.) + О2 (г.) = 2СО2 (г.) + 566,5 кДж
вычислите теплоту сгорания оксида углерода(II).
Ответ. 283,25кДж/моль
7. При сжигании 93 г белого фосфора выделилось 2322 кДж теплоты. Рассчитайте теплоту образования оксида фосфора(V).
Ответ. 1548кДж/моль
8. Вычислите тепловой эффект реакции
Fe2O3 + 2Al 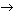 Al2O3 + 2Fe,
Al2O3 + 2Fe,
если теплота образования оксида железа(III) составляет +821,5 кДж/моль, а теплота образования оксида алюминия +1675,7 кДж/моль (теплота образования простого вещества равна нулю). Ответ. 854,2кДж/моль
 2015-07-21
2015-07-21 2648
2648






