Строго говоря, все реакции являются обратимыми. К практически необратимым реакциям можно отнести те, которые характеризуются большой величиной константы равновесия. Можно принять, что они протекают только в прямом направлении. При разработке технологии проведения процесса, основанного на необратимых реакциях, преследуют две основные цели: повышение скорости реакции и выхода целевого продукта. Ускорить необратимую реакцию возможно за счет увеличения начальных концентраций реагентов и путем повышения температуры процесса. Но главным способом ускорения необратимой реакции является правильный подбор катализатора процесса. Выход продукта в таких процессах пропорционален степени превращения сырья.
При разработке технологии проведения сложной необратимой реакции большое внимание уделяют повышению селективности процесса. Эта цель достигается подбором оптимальных концентраций реагентов и температур, а также подбором наиболее селективных катализаторов.
Селективность S реакции можно оценить соотношением (5.35) скоростей основной и побочной реакций:
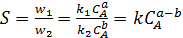 , (5.35)
, (5.35)
где k = k 1 /k 2.
На основе данного уравнения можно сделать выводы о влиянии концентрации на селективность:
– при a > b (порядок целевой реакции выше побочной) селективность пропорциональна максимальному значению концентрации;
– при a < b селективность пропорциональна минимальным значениям концентрации;
– при a = b концентрация не влияет на селективность
Катализ – наиболее сильное воздействие на селективность реакции. Катализ – сложная система реакций, при которых снижаются многие затруднения в протекании реакции по сравнению с некатализируемым процессом. Этот эффект связан с понижением энергии активации и/или увеличением предэкспоненциального множителя в кинетическом уравнении реакции.
 2015-08-21
2015-08-21 806
806








