1. Записати вихідні дані експерименту: r 0 = (9,990 ± 0,005)102 кг/м3; r =
= (7,140 ± 0,005)102 кг/м3; m = (76,0 ± 0,1) кг/кмоль; V 0 = (22,40 ± 0,05)10-3 м3.
2. Відкрити крани 4 й 5 і переконатись, що різниця рівнів води в колінах манометра дорівнює нулю.
3. Закрити кран 4, набрати в шприц порцію ефіру заданого викладачем об’єму V і ввести його в посудину через голку 3 (для забезпечення герметичності шприц із голки не виймати).
4. Спостерігати за показами манометра 6, очікуючи, коли рівні води в його колінах перестануть змінюватись. Виміряти різницю рівнів води h у колінах манометра і записати в таблицю:
| Номер за пор. | V, м3 | D V, м3 | h, м | D h, м |
| …. | ||||
| С.з. |
5. Відкрити кран 4 на 5–7 хв для провітрювання посудини.
6. Повторити дослід ще двічі згідно з пунктами 2–4.
7. Виміряти і записати значення кімнатної температури Т =(...±...)К.
8. Обчислити за формулами (6) і (2) k і R у кожному досліді. Результати усереднити.
9. Похибки вимірювань обчислити за формулами
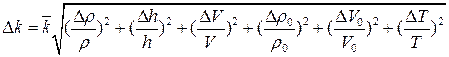 ;
;
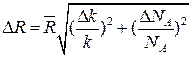 .
.
10. Записати кінцевий результат експерименту у вигляді
k =`k ±` D k, Ek = …%;
R =`R ±` D R, ER = …%.
Контрольні запитання
1. Який газ називають ідеальним?
2. Сформулюйте і поясніть закон Дальтона.
3. Запишіть і поясніть рівняння Менделєєва–Клапейрона.
4. Запишіть і поясніть основне рівняння молекулярно-кінетичної теорії газів.
5. Чим зумовлений тиск газу на стінку посудини і від чого він залежить?
6. Для чого в цій роботі використовують рідини, які легко випаровуються за кімнатної температури?
7. Сформулюйте і запишіть закони, які описують ізопроцеси в ідеальному газі.
8. У чому полягає фізичний зміст універсальної газової сталої? Як її обчислити?
Лабораторна робота №211. ВИЗНАЧЕННЯ СЕРЕДНЬОЇ ДОВЖИНИ ВІЛЬНОГО ПРОБІГУ ТА ЕФЕКТИВНОГО ДІАМЕТРА МОЛЕКУЛ ПОВІТРЯ
Завдання: визначити експериментально середню довжину вільного пробігу та ефективний діаметр молекул повітря шляхом дослідження його проходження через вузький капіляр.
Приладдя: установка для визначення довжини вільного пробігу молекул повітря; секундомір; термометр; барометр.
Теоретичний матеріал, який необхідно засвоїти під час підготовки до виконання роботи: основне рівняння молекулярно-кінетичної теорії (МКТ) газів; довжина вільного пробігу та ефективний діаметр молекул; середня, середня квадратична та імовірніша швидкість молекул; розподіл молекул за швидкостями; рівняння стану ідеального газу; внутрішнє тертя в газах; формула Пуазейля.
 Література:
Література:
1). § 15.1, c. 263–269; § 14.8, c. 251–255;
2). § 13.1, c. 9–12; § 13.5, c. 17–22;
§ 13.10, c. 27–29;
3). § 42–43, с. 129–138;
4). § 42–44, с. 75–78, § 46,48, с. 81–85.
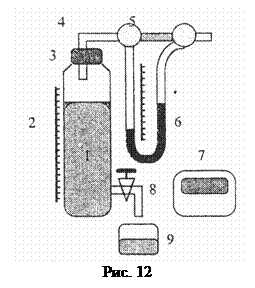
Опис установки. Установка для визна-чення довжини вільного пробігу молекул
газу (рис. 12) містить циліндричну посудину 1, заповнену дистильованою водою і щільно закриту корком 3. Через корок проходить скляна трубка 4, з’єднана з капіляром 5. Манометр 6 призначений для вимірювання різниці тисків повітря на кінцях капіляра 5. В нижній частині посудини 1 розміщений зливний кран 8, за допомогою якого вода з посудини може повільно витікати в мірну склянку 9. Зміну рівня води в посудині 1 вимірюють за допомогою лінійки 2. Секундомір 7 призначений для вимірювання часу проходження повітря через капіляр 5.
Ідея роботи та виведення робочих формул. Молекули газу рухаються хаотично і стикаються одна з одною. Шлях, який молекула проходить між двома послідовними зіткненнями, називають довжиною вільного пробігу l, а мінімальну відстань, на яку зближуються молекули під час зіткнення, – ефективним діаметром молекули de. Мікропараметри газу (розмір і маса молекул, швидкість, довжина вільного пробігу та ін.) пов’язані з макропараметрами (тиск, об’єм, температура) рівняннями молекулярно-кінетичної теорії. Отже, вимірявши макропараметри газу, можна за відповідними співвідношеннями розрахувати його мікропараметри.
Згідно з МКТ, коефіцієнт динамічної в’язкості газів
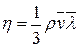 , (1)
, (1)
де h – коефіцієнт динамічної в’язкості; r – густина; ` v – середня швидкість теплового руху молекул.
Величина` v залежить від температури Т і молекулярної маси газу m:
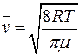 , (2)
, (2)
де R – універсальна газова стала.
Густину газу r можна розрахувати, користуючись рівнянням Менделєєва–Клапейрона 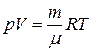 ,або
,або 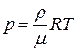 , оскільки
, оскільки 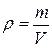 . Звідси
. Звідси
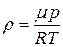 . (3)
. (3)
Тут P, V і Т – тиск, об’єм і температура газу; m – маса газу.
Якщо газ проходить через капіляр довжиною l і радіусом r, то його коефіцієнт в’язкості h, як і для рідин, визначають за формулою Пуазейля
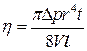 , (4)
, (4)
де D P – різниця тисків на кінцях капіляра; t – час протікання газу об’ємом V через капіляр. Підставимо вирази (2)–(4) в (1), отримаємо рівняння, з якого обчислимо` l:
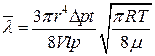 . (5)
. (5)
Величину D P в цій роботі визначають за допомогою манометра 6:
D P=rgh,(6)
а V – за зміною рівнів води в посудині 1:
V = S (H 1 – H 2), або 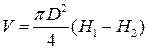 , (7)
, (7)
де D – внутрішній діаметр посудини 1; Н 1 і Н 2 – висоти рівнів води в посудині на початку і в кінці вимірювання.
Підставимо (6) і (7) у (5), отримаємо
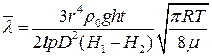 ,
,
або 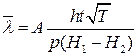 , (8)
, (8)
де А – стала приладу (зазначена в паспорті).
Розрахуємо тепер ефективний діаметр молекули повітря. З молекулярно-кінетичної теорії газів відомо, що
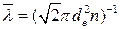 , (9)
, (9)
де n – концентрація молекул, яку можна визначити з рівняння стану ідеального газу р = nkТ, звідки
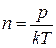 , (10)
, (10)
де k =1,38 · 10 -23 Дж/К – стала Больцмана.
Підставимо (10) у (9) і розв’яжемо отримане рівняння відносно de, матимемо
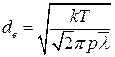 . (11)
. (11)
Вирази (8) і (11) є робочими формулами лабораторної роботи.
 2015-08-21
2015-08-21 338
338








