n Механизм действия ингибиторов:
n ингибитор взаимодействует с апоферментом: связывание функциональных групп белка, изменение третичной и четвертичной структуры апофермента, специфическое
связывание с определенным участком апофермента, неспецифическая
адсорбция на белке;
n ингибитор образует комплекс с субстратом;
n ингибитор связывает кофермент;
n ингибитор связывает активатор;
n ингибитор связывает кофактор.
Существует 3 типа ингибирования:
Конкурентное ингибирование – ингибитор имеет сходную структуру с субстратом и связывается с ферментом в активном центре. При этом максимальная скорость реакции не снижается, а величина Км увеличивается. Таким образом сродство фермента к субстрату снижается.
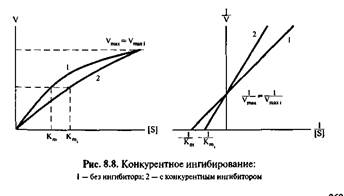
Неконкурентное ингибирование - ингибитор связывается с ферментом в аллостерическом центре. При этом максимальная скорость реакции снижается, а величина Км остается неизменной.
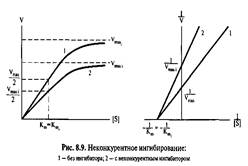
Смешанное ингибирование – связывание фермента и ингибитора происходит в активном и ином центре. При этом максимальная скорость реакции снижается, а величина Км повышается.
 2015-09-06
2015-09-06 439
439








