В 1925 г. шведский ученый В.Паули сформулировал положение, названное принципом Паули, согласно которому в атоме не может быть двух электронов с одинаковыми значениями всех четырех квантовых чисел (или: у которых все четыре квантовых числа были бы одинаковыми).
В соответствии с принципом Паули на одной атомной орбитали, характеризующейся определенными значениями трех квантовых n, 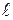 ,
, 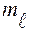 чисел, могут находиться только два электрона, отличающиеся значениями спинового квантового числа (
чисел, могут находиться только два электрона, отличающиеся значениями спинового квантового числа (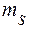 = +
= + 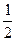 и
и 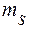 = -
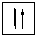
= - 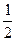 ), т.е. электроны с анти-параллельными спинами:. Такие электроны называются спаренными, в отличие от одиночного (т.е. неспаренного) электрона, занимающего какую-либо орбиталь.
), т.е. электроны с анти-параллельными спинами:. Такие электроны называются спаренными, в отличие от одиночного (т.е. неспаренного) электрона, занимающего какую-либо орбиталь.
 Пользуясь принципом Паули, можно подсчитать, какое максимальное число электронов может находиться на различных энергетических уровнях и подуровнях в атоме.
Пользуясь принципом Паули, можно подсчитать, какое максимальное число электронов может находиться на различных энергетических уровнях и подуровнях в атоме.
Поскольку каждый энергетический уровень включает n 2 орбиталей (n – главное квантовое число), то его емкость равна 2 n 2, т.е. по мере удаления от ядра емкость уровней увеличивается и составляет 2 (n = 1), 8 (n = 2), 18 (n =3), 32 (n = 4) … электронов (табл. 1).
Таблица 1
Квантовые состояния электронов,
емкость энергетических уровней и подуровней
| Энергети-ческий уровень | Энергети-ческий подуровень | Возможные значения магнитного квантового числа ml | Число орбиталей | Максимальное число электронов | ||
| в поду-ровне | в уров-не | на поду-ровне | на уров-не | |||
| К (n =1) | s (l =0) | |||||
| L (n =2) | s (l =0) p (l =1) | +1,0,–1 | ||||
| M (n =3) | s (l =0) p (l =1) d (l =2) | +1,0,–1 +2,+1,0,–1,–2 | ||||
| N (n =4) | s (l =0) p (l =1) d (l =2) f (l =3) | +1,0,–1 +2,+1,0,–1,–2 +3,+2,+1,0,–1,–2, –3 |
Число орбиталей на подуровне совпадает с числом значений ml и равно (2 l +1), поэтому на каждом подуровне максимально может находиться 2(2 l +1) электронов.
На s -подуровне (l = 0) в одной орбитали могут находиться максимально 2 электрона; на р -подуровне (l = 1) три атомных орбитали и максимально шесть электронов; на d -подуровне (l = 2) пять атомных орбиталей и десять электронов; на f -подуровне (l = 3) семь атомных орбиталей и максимальная емкость подуровня – четырнадцать электронов (табл. 1).
 2015-10-16
2015-10-16 2637
2637








