1. Жидкостями называются тела, которые имеют определенный объем, но не имеют своей формы, принимают форму сосуда, в котором они находятся. Они резко отличаются от газа и твердого тела.
Газ не имеет ни своего объема, ни своей формы (и то и другое зависит от сосуда, в котором находится газ). Твердое тело имеет свой объем и свою форму. Это различие обусловлено характером теплового движения молекул и силами молекулярного взаимодействия.
В жидкостях среднее расстояние между молекулами того же порядка, что и их размеры, поэтому перемещение молекул в объеме крайне затруднено. Движение молекул можно представить так: молекула жидкости в течение некоторого времени колеблется около определенного положения равновесия, затем под воздействием окружающих молекул она скачком меняет место равновесия, перемещаясь на расстояние порядка размера молекулы. Таким образом, молекулы жидкости можно разделить на две группы: одна из них газоподобна и совершает беспорядочные перемещения (кочующие молекулы), другая находится в колебательном движении (оседлые молекулы). Между оседлыми и кочующими молекулами существует динамическое равновесие. С ростом температуры возрастает доля кочующих молекул.
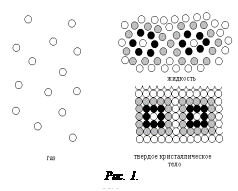 Газообразное, жидкое и твердое (кристаллическое) состояния вещества различаются степенью упорядоченности пространственного расположения частиц. Схематическое расположение частиц в газе жидкости и твердом кристаллическом теле показано на рис.1.
Газообразное, жидкое и твердое (кристаллическое) состояния вещества различаются степенью упорядоченности пространственного расположения частиц. Схематическое расположение частиц в газе жидкости и твердом кристаллическом теле показано на рис.1.
В газах молекулы располагаются совершенно неупорядоченно. В твердом теле частицы тела плотно упакованы и образуют кристаллические решетки, для которых характерна полная упорядоченность (дальний порядок). Жидкости обладают частично упорядоченной структурой (ближний порядок). Число ближайших соседей у фиксированных молекул будет примерно таким же, как и у частиц твердого тела, однако на далеких расстояниях расположение молекул жидкости будет не упорядоченным.
Если в твердом теле кристаллическая решетка сохраняется со временем, то в жидкости структура ближнего порядка непрерывно меняется вследствие малости времени оседлой жизни молекул (t» 10–11 с).
Жидкости, как и газы, обладают текучестью, любая неуравновешенная сила вызывает их течение. Это свойство коренным образом отличает их от твердых тел, где текучесть может проявиться под воздействием только сил, превосходящих предел упругости. Текучестью жидкости объясняется тот факт, что в широких сосудах, находящихся в поле силы тяжести, ее поверхность горизонтальна. Если жидкость освободить от действия силы тяжести, то она примет форму шара.
2. Внутреннее давление в жидкости.
На каждую молекулу со стороны окружающих ее молекул действует сила притяжения на расстоянии R. Проведенную сферу этим радиусом называют сферой молекулярного действия.
Каждая молекула взаимодействует только с непосредственно прилегающими к ней молекулами (на рис.1 это выделенные цветом молекулы).
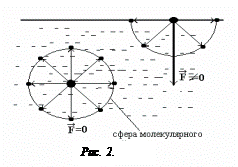 Рассмотрим молекулы жидкости, которые находятся на поверхности и внутри (рис.2). Молекула, которая находится внутри жидкости, со всех сторон окружена такими же молекулами. В результате результирующая сила притяжения равна нулю
Рассмотрим молекулы жидкости, которые находятся на поверхности и внутри (рис.2). Молекула, которая находится внутри жидкости, со всех сторон окружена такими же молекулами. В результате результирующая сила притяжения равна нулю 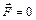 .
.
Иначе обстоит дело с молекулой, находящейся на поверхности (рис 2.) жидкости. Так как концентрация молекул в газе намного меньше концентрации молекул в жидкости (расстояние между молекулами в газе намного больше, чем в жидкости и взаимодействием между молекулами в газе можно пренебречь), то результирующая сила 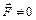 и направлена внутрь жидкости перпендикулярно ее поверхности. В результате поверхностный молекулярный слой жидкости будет оказывать на всю жидкость давление, равное сумме результирующих сил поверхностных молекул. Это давление называется внутренним или молекулярным.
и направлена внутрь жидкости перпендикулярно ее поверхности. В результате поверхностный молекулярный слой жидкости будет оказывать на всю жидкость давление, равное сумме результирующих сил поверхностных молекул. Это давление называется внутренним или молекулярным.
Оно оказывается огромным, что объясняет несжимаемость жидкости. Молекулы в жидкости оказываются сжатыми на таком расстоянии, что небольшое уменьшение расстояния между молекулами приводит к резкому возрастанию сил межмолекулярного отталкивания.
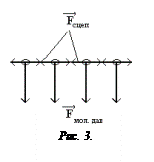 Силы сцепления между молекулами поверхности приводят к поверхностному натяжению (рис.3).
Силы сцепления между молекулами поверхности приводят к поверхностному натяжению (рис.3).
Поверхностное натяжение стремится сократить свободную поверхность жидкости, поэтому поверхность подобна растянутой упругой пленке, в которой возникает сила поверхностного натяжения, которая:
1. Направлена по касательной к поверхности.
2. Перпендикулярна произвольной линии, проведенной по поверхности жидкости.
3. Пропорциональна длине линии
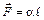 . (1)
. (1)
где 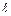 – длина линии на поверхности жидкости, a – коэффициент поверхностного натяжения.
– длина линии на поверхности жидкости, a – коэффициент поверхностного натяжения.
Коэффициент поверхностного натяжения численно равен силе поверхностного натяжения, действующей на единицу длины линии, ограничивающей поверхность жидкости. Единица измерения [a] = [Н/м].
Коэффициент поверхностного натяжения, а следовательно, и сила поверхностного натяжения, зависят от химического состояния жидкости и от ее температуры. С ростом температуры расстояние между молекулами возрастает, а силы межмолекулярного взаимодействия падают, что приводит к уменьшению силы и коэффициента поверхностного натяжения.
 2015-10-16
2015-10-16 517
517








