Определение качества воды
Качество воды, предназначенной для технологических целей, имеет большое значение. Качество воды определяют по комплексу органолептических, физико-химических и бактериологических показателей в соответствии с требованиями ГОСТ 2874 «Вода питьевая».
Правила отбора проб воды.
1. Пробу воды из водопровода отбирают в месте ее наибольшего расхода и в момент наибольшего расхода воды. В течение 5 мин воду спускают из крана, бутыль 3 раза ополаскивают водой, после чего набирают 2-3 л и закрывают бутыль пробкой.
2. Проба воды из водоема отбирается с глубины 75-100 см в бутыль с грузом.
6.1. Определение температуры.
Проведение испытания:
Температура замеряется через 5-10 мин после спуска воды из крана с точностью до 0,10С.
6.2. Определение запаха и вкуса.
Запах определяется органолептически.
Проведение испытания:
Определение запаха воды проводят при температуре 15-200С. Воду наливают в широкогорлую колбу емкостью 150-200 мл до 2/3 объема, накрывают часовым стеклом и взбалтывают вращательными движениями, после чего снимают стекло и быстро испытывают запах.
Запах определяется по балльной системе:
| 0 – отсутствует | 3 – заметный |
| 1 – очень слабый | 4 – отчетливый |
| 2 – слабый | 5 – очень сильный |
Запах при температуре 200С не должен быть более 2 баллов.
При проведении испытания воздух помещения должен быть чистым (без запаха), также необходимо обеспечить отсутствие запаха от рук и одежды наблюдателя.
Запах в воде может быть естественного происхождения (от грунта, растительности, живых организмов), например, болотный, травянистый, илистый, и искусственного – (от промышленных сточных вод и обработки воды химическими реагентами), например, фенольный, хлорный, нефтепродуктов.
Вкус также определяется органолептически.
Проведение испытания:
Для определения вкуса воду набирают в рот малыми порциями, не проглатывая, и задерживают на 3-5 с. Различают соленый, кислый, горький и сладкий вкус. Прочие ощущения называются привкусами. Интенсивность вкуса и привкуса определяют по вышеизложенной балльной системе (при температуре 200С вкус не должен быть более 2 баллов). Вкус определяют у сырой воды, за исключением случаев, когда вода является сомнительной в санитарном отношении. В таком случае воду кипятят, охлаждают до комнатной температуры и определяют вкус. При записи результатов отмечают «вкус кипяченой воды».
6.3. Определение прозрачности.
Проведение испытания:
Прозрачность определяется визуально путем сравнения с дистиллированной водой и количественно в цилиндре Генера. Цилиндр Генера имеет плоское дно, градуирован по высоте и у дна снабжен краном для спуска воды. Нефильтрованную воду хорошо взбалтывают и наливают в цилиндр, который ставят на страницу со стандартным шрифтом. Затем через кран спускают воду до тех пор, пока через оставшийся в цилиндре столб воды ясно не обозначится шрифт. Столб воды в цилиндре, отсчитанный в сантиметрах, выражает степень прозрачности. Во избежание оседания мути на дно цилиндра определение проводят как можно быстрее. Прозрачность питьевой воды по шрифту должна быть не менее 30 см.
6.4. Определение реакции воды.
Изменение окраски воды при добавлении к ней индикаторов характеризует реакцию воды, т.е присутствие в ней ионов 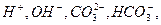 обуславливающих ту или иную величину рН. Реакцию воды обычно определяют по метиловому оранжевому, который имеет красную окраску в кислой среде и оранжево-желтую – в щелочной и изменяет окраску при рН 3,6 (3,1-4,4), и по фенолфталеину, который бесцветен в кислой среде, имеет малиновую окраску – в щелочной и изменяет окраску при рН 8,3 (8,2-10).
обуславливающих ту или иную величину рН. Реакцию воды обычно определяют по метиловому оранжевому, который имеет красную окраску в кислой среде и оранжево-желтую – в щелочной и изменяет окраску при рН 3,6 (3,1-4,4), и по фенолфталеину, который бесцветен в кислой среде, имеет малиновую окраску – в щелочной и изменяет окраску при рН 8,3 (8,2-10).
Проведение испытания:
В пробирку с водой добавляют 3-5 капель индикатора и, наблюдая за окраской, отмечают один из следующих вариантов:
| Вариант | Вода содержит ионы |
| 1. Вода желтая с метиловым оранжевым и розовая с фенолфталеином | 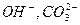
|
| 2. Вода желтая с метиловым оранжевым и бесцветная с фенолфталеином | 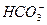
|
| 3. Вода оранжевая с метиловым оранжевым и бесцветная с фенолфталеином | 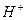
|
6.5. Определение рН.
Величину рН измеряют на рН-метре. рН питьевой воды по ГОСТ 2874 должен находиться в пределах 6,5-8,5.
6.6. Определение содержания взвешенных веществ (мутности).
Проведение испытания:
В бюксу с притертой крышкой укладывают плотный складчатый фильтр (Æ 9-11 см) и сушат до постоянной массы при температуре 1050С. Тщательно взболтанную воду отливают в несколько приемов в мерный стакан до метки «100 мл». Воду фильтруют через фильтр, пользуясь воронкой Бюхнера, колбой Бунзена и водоструйным насосом. Фильтр складывают в ту же бюксу и высушивают до постоянной массы при температуре 1050С.
Мутность воды (М) в мг/л определяют по формуле:
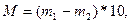
где m1 – масса бюксы и фильтра со взвешенными веществами, мг;
m2 – масса бюксы и пустого фильтра, мг;
Вычисление производят с точностью до 0,1 мг/л.
Мутность питьевой воды по ГОСТ 2874 не должна превышать 1,5 мг/л.
Профильтрованную воду используют для определения содержания сухого остатка (п. 6.7.)
6.7. Определение содержания сухого остатка.
Проведение испытания:
100 мл профильтрованной воды выпаривают в предварительно высушенной до постоянной массы и взвешенной фарфоровой чашке. Затем чашку с сухим остатком высушивают до постоянной массы при температуре 1050С и взвешивают.
Содержание сухого остатка (Х) в мг/л определяют по формуле:
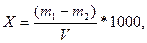
где m1 – масса чашки с сухим остатком, мг;
m2 – масса пустой чашки, мг;
V – объем воды, взятой для анализа, мл
Вычисление производят с точностью до 0,1 мг/л.
Содержание сухого остатка в питьевой воде по ГОСТ 2874 не должно превышать 1000 мг/л.
6.8. Определение окисляемости марганцевокислым калием.
Окисляемость марганцевокислым калием является условным показателем, характеризующим содержание в воде восстановителей (окисляющихся веществ).
Окисляемость определяют на холоде и при нагревании. Первая характеризует содержание в воде легкоокисляемых веществ (закисного железа, сульфидов, сульфитов, нитритов и т.д.), вторая – более трудноокисляемых органических веществ.
Окисляемость выражают количеством миллиграммов марганцевокислого калия или количеством миллиграммов кислорода, идущего на окисление веществ, содержащихся в 1 л исследуемой воды.
Сущность метода состоит в том, что марганцевокислый калий, будучи сильным окислителем, реагирует в присутствии серной кислоты с содержащимися в воде восстановителями:
2КMnO4 + 3H2SO4 = 2MnSO4 + K2SO4+ 3H2O + 5O
Избыток марганцевокислого калия связывается с вводимой в раствор щавелевой кислотой:
5С2Н2О4 + 2КMnO4 + 3H2SO4 = 2MnSO4 + К2SO4 + 8H2O + 10СO2
Не вступившая в реакцию избыточная щавелевая кислота оттитровывается обратно раствором марганцевокислого калия.
Проведение испытания:
В коническую колбу емкостью 250 мл наливают пипеткой 100 мл исследуемой воды, прибавляют 5 мл серной кислоты (1:3) и из бюретки 10 мл 0,01 н раствора марганцевокислого калия. Полученную смесь выдерживают 10 мин при комнатной температуре (если окисляемость определяется на холоде) или нагревают до кипения на водяной бане и кипятят 10 минут (если окисляемость определяется при нагревании). Затем в колбу приливают 10 мл 0,01 н раствора щавелевой кислоты и обесцветившийся раствор титруют 0,01 н раствором марганцевокислого калия до появления стойкого бледно-розового окрашивания. Во втором случае титруют горячий раствор.
Отметив количество израсходованного на титрование марганцевокислого калия (V1), добавляют еще 10 мл 0,01 н раствора щавелевой кислоты, чтобы установить соотношение между растворами, и обесцветившийся раствор титруют 0,01 н раствором марганцевокислого калия до появления стойкого бледно-розового окрашивания.
Окисляемость (О) в мг КMnO4/л воды определяют по формуле:
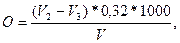
где V2 – общее количество 0,01 н раствора марганцевокислого калия, прибавленного к воде в начале опыта и израсходованного на титрование избытка щавелевой кислоты (10+ V1), мл;
V3 – количество 0,01 н раствора марганцевокислого калия, израсходованного на титрование 10 мл 0,01 н раствора щавелевой кислоты, мл;
V – объем воды, взятой для анализа, мл;
0,32 – количество КMnO4, соответствующее 1 мл 0,01 н раствора, мг.
Для условного выражения окисляемости в мг О2/л результат делят на 4.
Вычисление проводят с точностью до 0,1 мг КMnO4/л.
6.9. Определение жесткости воды.
Жесткость воды обуславливается содержанием в ней солей щелочноземельных металлов (кальция и магния), и выражается в микромолях на 1 л воды или в условных единицах – градусах. Один градус жесткости соответствует содержанию 0,01 г оксида кальция в 1 л воды. Содержащиеся в воде соли магния пересчитывают на оксид кальция.
Различают общую, постоянную и устранимую жесткость.
Общая жесткость – это общее количество солей кальция и магния в исследуемой (не кипяченой) воде.
Постоянная жесткость – это количество тех же солей, оставшихся после кипячения воды в течение 1 часа.
Устранимая жесткость – это содержание солей, осаждающихся при кипячении воды. Согласно ГОСТ 2874 общая жесткость не должна превышать 7 мкмоль/л.
Общую жесткость определяют методом трилонометрического титрования. Трилон Б, являющийся двунатриевой солью этилендиаминтетрауксусной кислоты (NаЭДТА), образует прочные комплексы с ионами двухвалентных металлов, в частности с ионами кальция и магния.
Проведение испытания:
В коническую колбу емкостью 250 мл пипеткой отмеряют такое количество воды, суммарное содержание ионов кальция и магния в котором не превышает 0,5 мкмоль/л. Для упрощения рекомендуется пользоваться данными таблицы 1.
Таблица 1
| Предполагаемая жесткость воды | Количество воды для анализа, мл | |
| мкмоль/л | град | |
| 0,5 – 5 | 1,4 – 14 | |
| 5 – 10 | 14 – 30 | |
| 10 – 20 | 30 – 56 | |
| 20 – 50 | 56 – 140 |
К отобранной пробе приливают дистиллированную воду, доводя количество содержимого колбы до 100 мл (если это необходимо), добавляют 5 мл аммиачного буферного раствора и 7-8 капель индикатора хромтемносинего. Содержимое колбы, интенсивно перемешивая, титруют 0,1 н раствором трилона Б до перехода окраски от винно-красной до синей с зеленоватым оттенком.
Аммиачно-буферный раствор готовят следующим образом: в мерной колбе на 1 л смешивают 100 мл 20%-го раствора NH4Cl и 100 мл 20%-го раствора NH3, доводят содержимое дистиллированной водой до метки. рН смеси должно быть равно 10.
Общую жесткость воды (ОЖ) в мкмоль/л воды определяют по формуле:
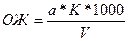
Общую жесткость воды (ОЖ) в градусах определяют по формуле:
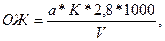
где а – количество 0,1 н раствора трилона Б, пошедшего на титрование, мл;
К – поправочный коэффициент для 0,1 н раствора трилона Б;
V – объем воды, взятой для анализа;
2,8 – количество миллиграммов оксида кальция, соответствующее 1 мл 0,1 н раствора трилона Б;
Вычисление производят с точностью до 0,01.
6.10. Определение содержания хлоридов.
Метод основан на осаждении хлор-иона в нейтральной или слабощелочной среде азотнокислым серебром.
Проведение испытания:
В пробирку наливают 5 мл исследуемой воды и добавляют 3 капли 10%-го раствора азотнокислого серебра. Примерное содержание хлор-иона определяют визуально в соответствии с таблицей 2.
Таблица 2
| Наблюдаемый эффект | Содержание хлор-иона, мг/л |
| Муть | 1 – 50 |
| Хлопья | 50-100 |
| Осадок | более 100 |
6.11. Определение содержания свободного (активного) хлора в хлорированной воде.
Хлорирование применяется с целью дезинфекции воды, а также для придания ей асептических свойств. Согласно ГОСТ 2874 содержание активного хлора в питьевой воде допускается в пределах от 0,3 до 0,5 мг/л.
Обнаружение активного хлора в воде основано на способности свободного хлора вытеснять йод из раствора йодистого калия в эквивалентном количестве. Выделившийся йод дает синее окрашивание с раствором крахмала. Количественное определение проводят путем титрования раствором серноватистокислого натрия.
2КJ + 2 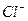 = 2J + 2KCl
= 2J + 2KCl
2J + 2Na2S2O3 = 2NaJ + Na2S4O6
Проведение испытания:
В коническую колбу на 250 мл наливают 5 мл 10%-го раствора йодистого калия добавляют 100 мл исследуемой воды, содержимое подкисляют путем добавления 2 мл серной кислоты (1:3). Содержимое колбы титруют 0,01 н раствором серноватистокислого натрия до получения слабой желтоватой окраски. Затем прибавляют 2-3 мл 1%-го раствора крахмала и продолжают титровать до полного исчезновения синего окрашивания.
Содержание свободного хлора (Х) в мг/л воды определяют по формуле:
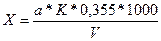 ,
,
где а – количество 0,01 н раствора серноватистокислого натрия, пошедшее на титрование, мл;
К – поправочный коэффициент для 0,01 н раствора серноватистокислого натрия;
0,355 – количество хлора, эквивалентное 1 мл 0,01 н раствора серноватистокислого натрия, мг;
V – объем воды, взятой для анализа, мл.
Вычисление проводят с точностью до 0,1 мг/л.
 2015-10-16
2015-10-16 405
405








