Две или несколько реакций в клетке иногда могут быть сопряжены таким образом, что общее изменение суммы их свободных энергий может обеспечить проведение процесса в благоприятном с позиций термодинамики направлении. В этих условиях изменение общей свободной энергии процесса – сумма индивидуальных изменений свободных энергий каждой реакции. Такой принцип сопряженных реакций действует на всех уровнях внутриклеточного обмена.
Посмотрим это на примере реакции фосфорилирования глюкозы - одной из важнейших клеточных реакций, с которой начинается использование глюкозы в клетке.
Глюкоза + Фн Û глюкоза-6-фосфат+ H2O
DGo' этой реакции + 14 кДж/моль, что указывает на невозможность самопроизвольного протекания этой реакции. Это эндэргоническая реакция. Однако эту реакцию можно представить в виде двух реакций
1. Глюкоза + Фн Û глюкоза-6-фосфат + H2O DGo' =+ 14 кДж/моль
2. ATФ + H2O Û AДФ + Фн, DG = - 31 kДж/моль, Это выраженная экзэргоническая реакция.
При суммировании двух реакций:
- Глюкоза + ATФ Û глюкоза-6-фосфат + AДФ DGo' = - 17 kДж/моль, что указывает на термодинамически благоприятное протекание реакции. Эта реакция катализируется в клетке ферментом гексокиназой
Таким образом, в обеспечении протекания в благоприятном с позиций термодинамики направлении реакций в клетке особую роль приобретают молекулы, реакция гидролиза которых характеризуется высокими отрицательными значениями DG. Такие соединения получили название макроэргических (высокоэнергетических) соединений или макроэргов.
|
|
|
Ведущие макроэрги в клетке - соединения, содержащие макроэргическую фосфатную группу.
Наиболее популярными макроэргами в клетке являются соединения, содержащие макроэргическую фосфатную группу. Для обозначения такой группы был введен специ 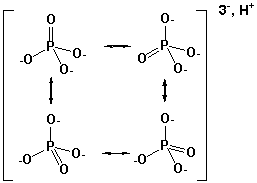 альный символ «~ Р» или «~Ф» означающий наличие макроэргической эфирной связи. Гидролиз фосфатной группы может сопровождаться изменением свободной энергии в диапазоне от -10 до -62 kДж/моль. (рис.). Такие величины изменений свободной энергии связаны с особенностями строения этих молекул, что выражается в:
альный символ «~ Р» или «~Ф» означающий наличие макроэргической эфирной связи. Гидролиз фосфатной группы может сопровождаться изменением свободной энергии в диапазоне от -10 до -62 kДж/моль. (рис.). Такие величины изменений свободной энергии связаны с особенностями строения этих молекул, что выражается в:
- Резонансной стабилизация фосфатсодержащих продуктов реакции.
На рисунке сверху показана резонансная стабилизация ортофосфата, HPO42- (сокращенно Фн). Существуют множественные резонансные формы, имеющие равную энергию, но они не все реализуются, когда фосфорнокислая группа связана в сложном эфире, типа ATP. Если же Фн высвобождается при гидролизе, множественные резонансные формы увеличивают полную энтропию системы, энергетически благоприятствуя процессу.
2. Дополнительной гидратации продуктов гидролиза. Высвобождение Фн создает большие возможности для гидратации. Гидратация - энергетически благоприятное состояние.
|
|
|
3. Электростатическом отталкивании между заряженными продуктами - Если оба про 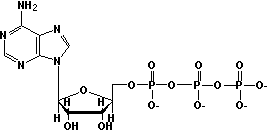 дукта гидролиза отрицательно заряжены (например, АДФ и Фн при гидролизе АТФ), отталкивание ионизированных продуктов способствует гидролизу. Заряженные фосфатные группы в ATФ тесно расположены друг около друга. Часть этого неблагоприятного электростатического взаимодействия уменьшается при превращении ATФ в AДФ; Равное количество освобождается, когда АДФ преобразуется в АМФ. Гидролиз АДФ имеет также DGo'= - 31 kДж/моль.
дукта гидролиза отрицательно заряжены (например, АДФ и Фн при гидролизе АТФ), отталкивание ионизированных продуктов способствует гидролизу. Заряженные фосфатные группы в ATФ тесно расположены друг около друга. Часть этого неблагоприятного электростатического взаимодействия уменьшается при превращении ATФ в AДФ; Равное количество освобождается, когда АДФ преобразуется в АМФ. Гидролиз АДФ имеет также DGo'= - 31 kДж/моль.
4. Повышенной резонансной стабилизации или таутомеризации продуктов реакции. - Гидролизу способствуют молекулы, способные принимать множественные молекулярные формы. Например, пировиноградная кислота имеет две молекулярные формы, в то время как фосфоенолпируват - только одну
5. Высвобождении протонов в окружающую среду – высвобождаемые протоны при некоторых реакциях гидролиза (см рис) оказывают влияние на реакцию.
Таблица 4-6. Стандартная свободная энергия гидролиза некоторых органических фосфатов, используемых в клетке.
| Соединение | DGo’ кДж/моль |
| Фосфоенолпируват | -61.9 |
| Карбамоилфосфат | -51.4 |
| 1,3 дифосфоглицерат | -49.3 |
| Креатинфосфат | -43.1 |
| АТФ→ АДФ+ Фн | -30.5 |
| АДФ→АМФ+Фн | -27.6 |
| Пирофосфат | -27.6 |
| Глюкоза-1-фосфат | -20.9 |
| Фруктоза-6-фосфат | -15.9 |
| АМФ | -14.2 |
| Глюкоза-6-фосфат | -13.8 |
| Глицерол-3-фосфат | -9.2 |
.
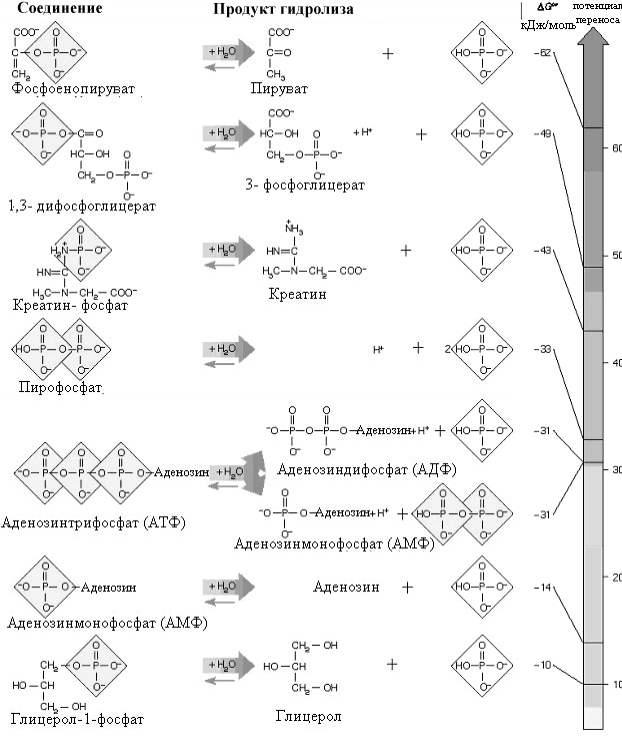
Рис. 4-4. Реакции гидролиза некоторых биохимически важных фосфат содержащих соединений.
Как видно из таблицы 4-6 и рис. 4-4 молекула АТФ разделяет все соединения с фосфоэфирной связью на две группы. Одна группа, расположенная на рис. 4-4 выше АТФ, имеет значения DGo’ значительно более высокие, чем у АТФ. Эту группу макроэргов можно разделить по типу химической связи на
· ангидриды (АТФ, АДФ, 1,3 дифосфоглицерат);
· енолфосфаты (фосфоенолпируват);
· фосфогуанидины(креатинфосфат, аргининфосфат);
· тиоловые эфиры (ацетил- КоА);
Соединения, расположенные ниже АТФ отличаются более низкими значениями DGo’ и как правило не называются макроэргами.
«Энергетической валютой» клетки является АТФ
Такое «центральное» расположение молекулы АТФ позволяет ей выполнять роль донора высокоэнергетического фосфата для соединений, расположенных ниже в таблице, превращаясь при этом в АДФ, а АДФ - роль акцептора высокоэнергетического фосфата у соединений, расположенных выше. Цикл АТФ/АДФ связывает, тем самым, процессы генерирующие «~Р» с процессами, использующими «~Р». Сумму всех адениловых нуклеотидов в клетке (АТФ,АДФ и АМФ) называют адениловой системой. Процессы гидролиза и синтеза АТФ происходят с высокой скоростью, поскольку общий фонд АТФ очень маленький и для поддержания процессов жизнедеятельности в клетке его хватает только на несколько секунд.
В клетках организмов животных есть три основных источника ~P для синтеза АТФ.
· окислительное фосфорилирование – механизм образования АТФ, использующий для этого энергию градиента электрохимического потенциала, возникающего на внутренней мембране митохондрий.
· Субстратное фосфорилирование – механизм синтеза АТФ, использующий энергию макроэргических соединений, образующихся в процессе метаболизма (1,3- дифосфоглицериновая кислота, сукцинил-КоА и т.д.).
· Синтез АТФ с использованием макроэргов, выполняющих своеобразную роль молекул – депо макроэргических связей (креатинфосфат).
Тому, каким образом живые системы преобразуют энергию поступающих из внешней среды химических соединений, в энергию макроэргических соединений и посвящена значительная часть курса биохимии.
[1] Конфигурация полимера - это такое расположение атомов полимерной молекулы в пространстве, изменить которое можно только после разрыва ковалентных связей.
|
|
|
[2] Гомологичными называются белки, которые выполняют одну и ту же функцию, но отличаются по структуре.
[3] Конформация полимера - это такое расположение атомов полимерной молекулы в пространстве, которое обусловлено вращением отдельных атомов или групп атомов этого полимера вокруг одинарных ковалентных связей.
 2015-10-16
2015-10-16 1128
1128








