Работа № 7
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Скорость химической реакции (v) характеризуется изменением количества реагирующего вещества за единицу времени в единице реакционного пространства.
В гомогенной (однородной по агрегатному состоянию) системе реакционным пространством служит объем сосуда, в котором происходит реакция.
Скорость гомогенной химической реакции измеряется по изменению концентрации за единицу времени для одного из веществ, участвующих в реакции. Концентрация (С) выражается обычно в моль/л, поэтому размерность скорости моль/л 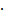 с. При химической реакции концентрация каждого из исходных веществ уменьшается во времени (С2<С1;
с. При химической реакции концентрация каждого из исходных веществ уменьшается во времени (С2<С1; 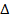 С<0), а концентрация каждого из продуктов реакции возрастает (С2>С1
С<0), а концентрация каждого из продуктов реакции возрастает (С2>С1 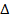 С>0).
С>0).
Различают два вида скорости — среднюю и истинную (или мгновенную). Средняя скорость (v) равна отношению:
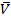 =
= 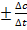
где 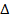 С=С2-
С=С2- 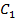 ;
; 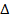 t=
t= 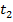 -t1.
-t1.
Чтобы величина скорости всегда была положительной перед дробью ставят знаки ±.
Истинная скорость химической реакции 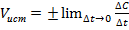
т. е. является производной концентрации по времени:
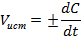
Скорость химических реакций зависит от многих факторов, важнейшие из них: природа реагирующих веществ, концентрация, давление (для реакций с участием газообразных веществ), температура, участие катализаторов.
Зависимость скорости реакции от концентрации реагирующих веществ выражается законом действия, масс. Формулировка закона: при постоянной температуре скорость химической реакции пропорциональна произведению концентраций реагирующих веществ, причем каждая концентрация входит в произведение в степени, равной коэффициенту, стоящему перед формулой данного вещества в уравнении реакции. Представим уравнение химической реакции в общем виде:
аА +bB = cC + dD.
Тогда закон действия масс можно записать в форме
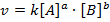
где [А] и [В] — молярные концентрации вступающих в реакцию веществ; а и b — коэффициенты в уравнении реакции; k —'константа скорости реакции, величина которой зависит от 'природы реагирующих веществ, температуры и присутствия катализаторов, но не зависит от концентраций веществ; k численно равна скорости реакции при [A]=[В]=1 моль/л.
Все химические реакции можно разделить на два типа: необратимые и обратимые. Реакции, которые протекают в одном направлении и идут до конца, называются необратимыми. Большинство реакций являются обратимыми, т. е. протекают в противоположных направлениях и не идут до конца. Изобразим обратимую реакцию в общем виде
аА+bВ 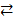 сС+dD
сС+dD
зависимости скорости прямой v1, и обратной v2 реакции от концентраций реагирующих веществ выражаются соотношениями:
v1=k1[A]a 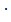 [B]b,v2 =k2[C]c
[B]b,v2 =k2[C]c 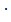 [
[ 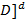 .
.
Состояние, при котором скорость прямой реакции равна скорости обратной, называется химическим равновесием, а концентрации четырех веществ—равновесными. Следовательно, когда vl = v2,
k1 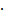 [A]a
[A]a 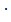 [B]b=k2
[B]b=k2 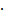 [C]c
[C]c 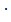 [
[ 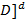 .
.
Отсюда
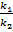 =
= 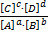 =R
=R
где К — константа химического равновесия реакции.
К в отличие от константы скорости химической реакции не зависит от катализатора, так как он в одинаковой степени изменяет скорости прямой и обратной реакций.
Переход системы из одного равновесного состояния в другое в результате изменения одного из условий равновесия (С, Р, Т) называется смещением химического равновесия. Смещение равновесия определяется принципом Ле Шателье: если в системе, находящейся в равновесии, изменить одно из условий, то происходит смещение равновесия в направлении той реакции, которая (противодействует указанному изменению. Применяя принцип Ле Шателье, можно сделать следующие выводы:
1. Увеличение концентрации одного из веществ вызывает смещение равновесия в сторону реакции, которая понижает концентрацию этого вещества.
2. Увеличение давления смещает равновесие в направлении уменьшения общего числа молей газообразных веществ, то есть в направлении, приводящем к понижению давления.
3. Нагревание смещает равновесие в сторону эндотермической реакции, охлаждение — в сторону экзотермической реакции.
 2015-10-16
2015-10-16 272
272







