Курсовая работа состоит из двух частей: теоретической и практической. Теоретическая часть содержит два теоретических вопроса (табл. 1). Практическая часть включает две задачи (табл. 2,3).
Таблица 1.
Вопросы теоретической части
| № варианта | Наименование вопроса |
| 1. Стадии и фазы развития пожара в помещении. | |
| 2. Механизм выгорания жидкости. | |
| 1. Тепловой баланс внутреннего пожара. | |
| 2. Дебит фонтанов и методы его оценки. | |
| 1. Характеристика порошковых огнетушащих составов. | |
| 2. Параметры газовых фонтанов. | |
| 1. Скорость развития внутреннего пожара. | |
| 2. Газовые фонтаны и их категории. | |
| 1. Очаг пожара, очаговые признаки. | |
| 2. Комбинированные и прочие средства тушения. | |
| 1. Тепловая теория прекращения горения. | |
| 2. Твердотопливные аэрозолеобразующие составы. | |
| 1. Физико-химические механизмы прекращения горения. | |
| 2. Химически активные ингибиторы. | |
| 1. Способы пожаротушения. | |
| 2. Инертные разбавители. | |
| 1. Характеристика воды, как огнетушащего вещества. | |
| 2. Пожары, регулируемые пожарной нагрузкой и вентиляцией. | |
| 1. Классификация огнетушащих веществ. | |
| 2. Характеристика огнетушащих пен. | |
| 1. Адсорбция. ПАВ. | |
| 2. Вскипание и выброс. | |
| 1. Смачивание и растекание жидкостей. | |
| 2. Виды теплопереноса | |
| 1. Причины и источники возгорания | |
| 2. Горение измельченных материалов | |
| 1. Электричество как причина пожара | |
| 2. Возгорание и самовозгорание | |
| 1. Параметры пожарной опасности веществ и материалов | |
| 2. Условия возникновения пожара | |
| 1. Режим развитого пожара. | |
| 2. Инертные разбавители. | |
| 1. Условия, необходимые для полного охвата помещения пламенем. | |
| 2. Очаг пожара, очаговые признаки | |
| 1. Факторы, влияющие на развитие пожара в помещении. | |
| 2. Особенности динамики пожаров на транспорте. | |
| 1. Стадии и фазы развития пожара в помещении. | |
| 2. Распространение пожара за пределы помещения. | |
| 1. Стадии и фазы развития пожара в помещении. | |
| 2. Тепловой баланс внутреннего пожара. | |
| 1. Факторы, влияющие на развитие пожара в помещении. | |
| 2. Характеристика порошковых огнетушащих составов. | |
| 1. Условия, необходимые для полного охвата помещения пламенем. | |
| 2. Динамика газообмена. | |
| 1. Скорость развития внутреннего пожара. | |
| 2.Тепловая теория прекращения горения. | |
| 1. Распространение пожара за пределы помещения. | |
| 2.Физико-химические механизмы прекращения горения. | |
| 1. Скорость развития внутреннего пожара. | |
| 2. Характеристика огнетушащих пен. | |
| 1. Динамика газообмена. | |
| 2. Характеристика воды, как огнетушащего вещества. | |
| 1. Тепловой баланс внутреннего пожара. | |
| 2. Характеристика порошковых огнетушащих составов. | |
| 1. Характеристика порошковых огнетушащих составов. | |
| 2. Характеристика огнетушащих пен. | |
| 1. Динамика газообмена. | |
| 2. Характеристика воды, как огнетушащего вещества. | |
| 1. Скорость развития внутреннего пожара. | |
| 2. Классификация огнетушащих веществ |
Задача 1. Рассчитать выгоревшую массу древесины на пожаре в складе штабеля древесины, определить следующие параметры пожара: теоретический и фактический расходы воздуха, массовую долю сгоревшего материала, коэффициент поверхности горения, положение плоскости равных давлений, а также определить относится ли данный тип пожара к регулируемому вентиляцией или пожарной нагрузкой. В табл. 2 приведены исходные данные для расчета. Вид штабеля приведен на рис.1.
Таблица 2.
Данные для решения задачи 1
| № пп | Плот-ность древе-сины ρ, кг/м3 | Дли-на бру-са l, м | Сече-ние а, м | Вре-мя горе-ния, τ, мин | Удель-ная массо-вая скоро-сть выгора-ния
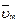 ,кг/(м2.с) ,кг/(м2.с)
| Температура окру-жаю-щей среды, Тос, ºС | Сре-дне-объ-ем-ная тем-пера-тура, Т, ºС | Давление, Р кПа | Коэф-фици-ент сопро-тив-ления про-ема μ | Разме-ры прое-ма, м |
| 1,0 | 0,10 | 0,010 | 101,3 | 0,7 | 0,5×2,0 | |||||
| 1,1 | 0,11 | 0,014 | 101,3 | 0,7 | 0,8×1,3 | |||||
| 1,2 | 0,12 | 0,018 | 101,3 | 0,7 | 0,8×2,0 | |||||
| 1,3 | 0,13 | 0,017 | 101,3 | 0,7 | 0,6×1,4 | |||||
| 1,4 | 0,14 | 0,010 | 101,3 | 0,7 | 0,9×1,8 | |||||
| 1,5 | 0,15 | 0,018 | 101,3 | 0,7 | 0,8×1,8 | |||||
| 1,6 | 0,16 | 0,018 | 101,3 | 0,7 | 0,6×1,5 | |||||
| 1,7 | 0,17 | 0,010 | 101,3 | 0,7 | 1,0×2,4 | |||||
| 1,8 | 0,18 | 0,015 | 101,3 | 0,7 | 1,0×1,8 | |||||
| 1,9 | 0,19 | 0,014 | 101,3 | 0,7 | 0,8×1,5 | |||||
| 2,0 | 0,20 | 0,013 | 101,3 | 0,7 | 1,2×2,4 | |||||
| 2,1 | 0,21 | 0,015 | 101,3 | 0,7 | 1,2×1,8 | |||||
| 2,2 | 0,22 | 0,012 | 101,3 | 0,7 | 0,8×1,6 | |||||
| 2,3 | 0,23 | 0,014 | 101,3 | 0,7 | 1,2×1,8 | |||||
| 2,4 | 0,24 | 0,011 | 101,3 | 0,7 | 1,2×2,0 | |||||
| 2,3 | 0,23 | 0,017 | 101,3 | 0,7 | 0,6×2,0 | |||||
| 2,2 | 0,22 | 0,015 | 101,3 | 0,7 | 0,8×2,0 | |||||
| 2,1 | 0,21 | 0,016 | 101,3 | 0,7 | 1,0×1,6 | |||||
| 2,0 | 0,20 | 0,013 | 101,3 | 0,7 | 0,8×1,9 | |||||
| 1,9 | 0,19 | 0,016 | 101,3 | 0,7 | 0,7×1,4 | |||||
| 1,8 | 0,18 | 0,012 | 101,3 | 0,7 | 1,2×1,5 | |||||
| 1,7 | 0,17 | 0,017 | 101,3 | 0,7 | 1,2×2,0 | |||||
| 1,6 | 0,16 | 0,018 | 101,3 | 0,7 | 0,8×1,5 | |||||
| 1,5 | 0,15 | 0,011 | 101,3 | 0,7 | 0,8×1,7 | |||||
| 1,4 | 0,14 | 0,012 | 101,3 | 0,7 | 0,6×1,2 | |||||
| 1,3 | 0,13 | 0,019 | 101,3 | 0,7 | 0,7×2,0 | |||||
| 1,2 | 0,12 | 0,014 | 101,3 | 0,7 | 0,6×1,8 | |||||
| 1,1 | 0,11 | 0,013 | 101,3 | 0,7 | 0,8×1,7 | |||||
| 2,4 | 0,24 | 0,016 | 101,3 | 0,7 | 1,0×2,5 | |||||
| 1,0 | 0,10 | 0,012 | 101,3 | 0,7 | 0,9×1,8 |
Задача 2. Рассчитать минимальную флегматизирующую концентрацию инертного разбавителя, об. %, исходя из значения минимальной адиабатической температуры горения паровоздушной смеси вещества А при разбавлении её флегматизатором Ф (см. табл. 3), построить зависимость нижнего и верхнего концентрационных пределов распространения пламени для смеси, а также определить минимальное взрывоопасное содержание кислорода, безопасную концентрацию кислорода и объем флегматизатора в составе предельной по горючести стехиометрической смеси. Адиабатическая температура горения смеси стехиометрического состава составляет 1500 K.
Таблица 3
Данные для решения задачи № 2
| Номер задания | Название вещества А | Химическая формула | Q н, кДж/моль | Флегматизатор Ф |
| 1 | 2 | 3 | 4 | 5 |
| Пентан | С5Н12 | Азот | ||
| Гексан | С6Н14 | Водяной пар | ||
| Пропанол - 1 | С3Н8О | Диоксид углерода | ||
| Водород | Н2 | 2 072 | Азот | |
| Бутан | С4Н10 | 2 010 | Водяной пар | |
| Метиловый спирт | СН4О | Диоксид углерода | ||
| Ацетон | СН3СОСН3 | Азот | ||
| Амиловый спирт | С5Н12О | Диоксид углерода | ||
| Пропилен | С3Н6 | Диоксид углерода | ||
| Аммиак | NH3 | 1 777 | Водяной пар | |
| Пропан | C3Н8 | 1 987 | Диоксид углерода | |
| Ацетилен | C2Н2 | 2 307 | Азот | |
| Толуол | С7Н8 | Диоксид углерода | ||
| Бензол | С6Н6 | Азот | ||
| Этан | С2Н4 | 1 922 | Диоксид углерода | |
| Этиловый спирт | С2Н6О | Диоксид углерода | ||
| Этилен | С2Н4 | 2 067 | Азот | |
| Сероводород | Н2S | Водяной пар | ||
| Диэтиловый эфир | С4Н10О | Диоксид углерода | ||
| Окись углерода | СО | 2 000 | Азот | |
| Уксусноэтиловый эфир | С4Н8О2 | Диоксид углерода | ||
| Бутанол - 1 | С4Н10О | Водяной пар | ||
| Метан | СН4 | 1 927 | Диоксид углерода | |
| Этиленгликоль | С2Н6О2 | Азот | ||
| Бензилбензоат | С14Н12О2 | Азот | ||
| Диэтилмалеат | С8Н12О4 | Водяной пар | ||
| Кетен | С2Н2О | Диоксид углерода | ||
| Нонилбензол | С15Н24 | Водяной пар | ||
| Этилпропиловый эфир | С5Н12О | Диоксид углерода | ||
| Фенол | С6Н6О | Азот |
Варианты задания определяются преподавателем.
Таблица 4
Средняя изобарная теплоёмкость основных продуктов горения в интервале температур 273 - 1500 K
| Вещество | Удельная теплоёмкость, С р, |
| кДж/(моль×K) | |
| Диоксид углерода | 5,08×10−2 |
| Диоксид серы | 5,11×10−2 |
| Вода (пар) | 3,99×10−2 |
| Азот | 3,18×10−2 |
| Воздух | 3,23×10−2 |
 2015-10-13
2015-10-13 545
545








