В физиологическом диапазоне рН оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Поэтому, освобождая в тканях кислород, восстановленный гемоглобин приобретает большую способность к связыванию ионов водорода.
Гемоглобиновый буфер обеспечивает 35% буферной емкости крови.
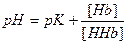
Гемоглобин является амфотерным веществом. В тканях редуцированный гемоглобин проявляет основные свойства:
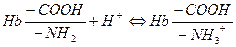
Оксигемоглобин, образующийся в легких, ведет себя как кислота, поэтому смещения рН в кислую сторону не происходит. В капиллярах НbО2 теряет часть кислотных свойств. Образующийся редуцированный гемоглобин связывает ионы водорода и освобождает ионы калия, которые при ацидозе выходят из эритроцитов, вызывают гиперкалиемию. Ионы калия затем выводятся почками.
Под влиянием избытка СО2 сродство гемоглобина к кислороду падает, а диссоциация оксигемоглобина повышается. Уменьшение емкости гемоглобинового буфера происходит при кровопотере, гемолизе, анемиях.
Концентрация водородных ионов почти полностью определяется соотношением бикарбоната и углекислоты. Содержание этих веществ в крови тесно связано с процессом переноса кровью углекислого газа (СО2) от тканей к легким. Физически растворенный СО2 диффундирует из тканей в эритроцит в соответствии с градиентом концентрации, поскольку в эритроцитах образуется мало углекислого газа. В эритроците под действием фермента карбоангидразы происходит гидратация молекулы СО2 с образованием угольной кислоты (Н2СО3), сразу же диссоциируя на ион бикарбоната и ион водорода:
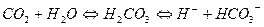
Накапливающийся ион НСО3ˉ диффундирует по градиенту концентрации в плазму. Электрохимическая нейтральность поддерживается за счет перемещения в эритроциты ионов хлора (хлоридный сдвиг).
В физиологических условиях повышение рСО2 в венозной крови стимулирует образование НСО3ˉ в эритроцитах. Наоборот, снижение рСО2 в артериальной крови угнетает образование бикарбоната. При этом обеспечивается постоянство артерио-венозной разницы НСО3ˉ/СО2 и, следовательно, рН.
При патологических процессах, сопровождающихся изменениями рСО2, эти механизмы сохраняются. Повышение рСО2 в эритроцитах способствует увеличению внеклеточного бикарбоната, и наоборот.
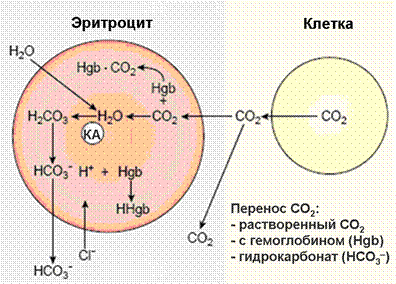
Рис.4.Химические реакции, протекающие в эритроцитах при газообмене в тканях.
Буферные свойства крови обусловлены, в конечном итоге, суммарным эффектом всех анионных групп слабых кислот, важнейшими из которых являются бикарбонаты и анионные группы белков. Эти анионы, обладающие буферными эффектами, получили названия «буферные основания» (buffer bases, BB).
Клетки являются постоянным источником углекислого газа и нелетучих кислот. Часть ионов водорода способна через метаболически активные механизмы поступать в клетки в обмен на ионы калия. В клеточном секторе преимущественное значение имеют фосфатная и белковая буферные системы. Буферные основания представлены в основном калийными солями фосфорной кислоты и белков.
Калиево-водородный обмен в плазме.
Свободное перемещение одноименно заряженных ионов калия (К+) и водорода (Н+) между внутриклеточным и внеклеточным секторами организма имеет важное значение в регуляции кислотно-основного равновесия. В случаях ацидоза избыточные ионы водорода мигрируют во внутрь клеток для буферирования. При этом, другой катион, а именно ион К+, покидает клетку и передвигается во внеклеточную жидкость. В случаях снижения уровня внеклеточного калия, ионы К+ перемещаются в клетки и заменяются ионами водорода. Таким образом, изменения уровней внеклеточного калия могут оказывать влияние на кислотно-основное состояние, и изменения кислотно-основного состояния влияют на уровни внеклеточного калия. Сдвиги калия, обыкновенно, более выражены при метаболическом ацидозе, чем при респираторном ацидозе. Следует отметить, что метаболический ацидоз, развивающийся в результате накопления неорганических кислот (например, HCl в случае диареи, фосфорной кислоты при почечной недостаточности), приводит к более значительному повышению калия во внеклеточном пространстве, чем ацидоз, вызываемый аккумуляцией органических кислот (например, лактата, кетокислот).
 2015-10-13
2015-10-13 2030
2030
