На основе приведенных выше соотношений были составлены предлагаемые таблицы термодинамических свойств газов. Оказалось целесообразным дать подробные таблицы для каждого компонента газовой смеси, с тем чтобы вести расчеты процессов как с отдельными газами, так и с различными газовыми смесями, в том числе и с продуктами сгорания топлив произвольного состава. При этом данные для газовой смеси определяются по данным для компонентов по простому правилу смешения (аддитивности).
При расчете процессов с продуктами сгорания практически придется пользоваться четырьмя таблицами (для N2, CO2, О2 и Н2О). Для воздуха составлена отдельная таблица. Приводится также таблица термодинамических свойств гелия, который может рассматриваться как перспективное рабочее тело газотурбинных установок для атомных электростанций.
В основу расчета таблиц термодинамических свойств газов положены новейшие значения теплоемкостей, вычисленные по спектроскопическим данным с учетом новых значений фундаментальных физических констант, а для водяного пара и двуокиси углерода — с учетом центробежной деформации молекул при их вращении.
В связи с возрастающим применением в теплотехнических расчетах электронных вычислительных машин (ЭВМ) найдено целесообразным значения теплоемкости газов аппроксимировать аналитическими зависимостями и использовать эти зависимости для составления таблиц.
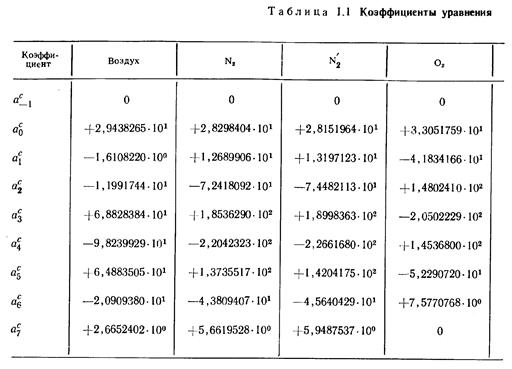
Значения теплоемкостей газов аппроксимированы на ЭВМ методом наименьших квадратов в виде полиномов от абсолютной температуры
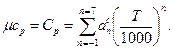 (13)
(13)
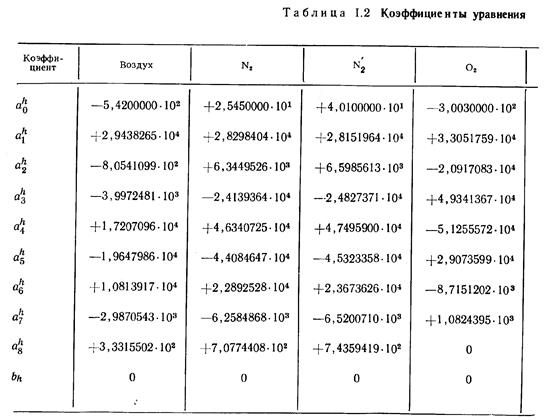
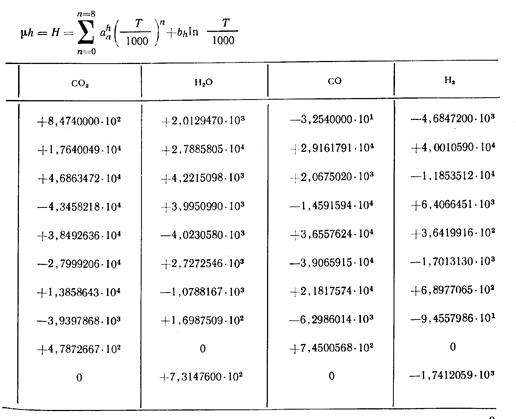
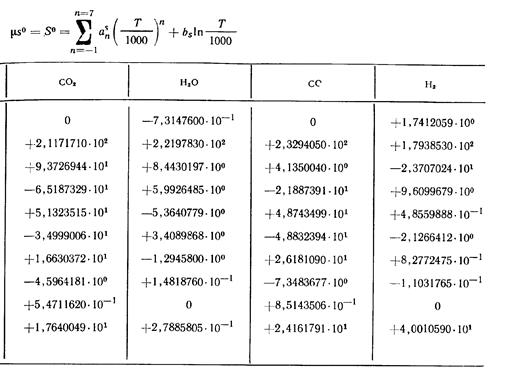
На основе известных термодинамических соотношений и выражения (13) для теплоемкостей найдены значения коэффициентов в выражениях для энтальпии и энтропии:
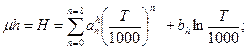 (14)
(14)
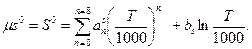 (15)
(15)
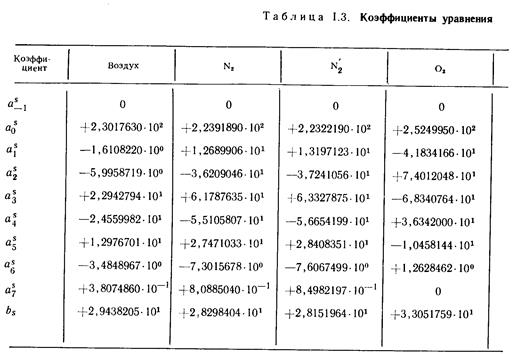
Значения коэффициентов уравнений (13), (14) и (15), использованных при составлении таблиц, приведены в табл. 1.1, 1.2 и 1.3.
Таблицы составлены в Международной системе единиц с интервалом в 1 °С и включают данные о термодинамических свойствах газов в области температур от —50 до +1500°С. В графе первой даны значения температуры t в градусах Цельсия, а в графе второй — значения абсолютных температур Т в кельвинах.
Далее в таблицах приводятся значения энтальпии h, кДж/кг, внутренней энергии и, кДж/кг, безразмерных величин — относительного давления π0 и относительного объема θ° и значения s°, кДж/(кг∙К):
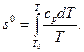 (16)
(16)
Часто при расчетах (в особенности с газовыми смесями) удобнее иметь значения калорических величин, отнесенные к 1 молю. Поэтому в последних трех графах таблиц приводятся значения энтальпии µh=Н, кДж/кмоль; внутренней энергии µu=U, кДж/кмоль, и µs° = S°, кДж/(кмоль∙К), для 1 моля газов.
За базовую температуру принят абсолютный нуль. В качестве стандартных приняты значения энтальпии и
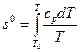
при температуре 298,15 °С. Значение универсальной газовой постоянной принято равным µR = 8314,41 Дж/(моль∙К).
Книга включает таблицы термодинамических свойств воздуха, азота, атмосферного азота, кислорода, водяного пара, диоксида углерода, оксида углерода, водорода и гелия.
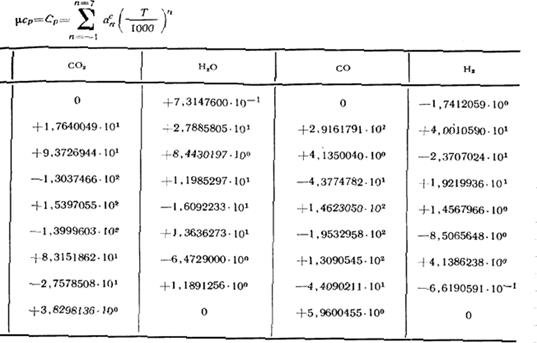
Для каждого из перечисленных газов приводится дополнительная таблица, включающая значения изобарной теплоемкости ср,кДж/(кг∙К), и µср = Ср, кДж/(кмоль∙К), изохорной теплоемкости cv, кДж/(кг∙К), µcv = Cv, кДж/(кмоль∙К), и показателя адиабаты k = cp/cv.
При составлении таблиц для воздуха и атмосферного азота принят следующий объемный состав:
Для воздуха Для атмосферного азота
Азот........................................ 0,7803 Азот........................................... 0,9876
Кислород....................... 0,2099 Аргон................................... 0,0119
Аргон................................. 0,0094 Диоксид углерода.............. 0,0004
Водород............................. 0,0001 Водород................................ 0,0001
Диоксид углерода............. 0,0003
 2015-10-13
2015-10-13 505
505








