1) 44,8 л 2) 22,4л 3) 67,2 4) 89,6л
4. В реакцию, протекающую в соответствии с термохимическим уравнением
2Al + 3S = Al2S3 +509 кДж вступило 108 г алюминия. Количество выделившейся теплоты равно____.
1) 242,5 кДж 2) 509 кДж 3) 1018 кДж 4) 2036 кДж
5. В результате реакции, термохимическое уравнение которой 2Al +Fe2O3 = Al2O3 + 2 Fe +848 кДж, выделилось 169,6 кДж теплоты. Масса образовавшегося железа равна_____.
1) 11,2 г 2) 22,4 г 3) 56 г 4) 28 г
6. По термохимическому уравнению реакции горения ацетилена 2С2Н4 + 5О2 = 4СО2 + 2Н2О +2610 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило 67,2 л ацетилена (н.у.)
1) 870 кДж 2) 3915 кДж 3) 5220 кДж 4) 7830 кДж
7. В результате реакции, термохимическое уравнение которой 2С2Н4+ 5О2 = 4СО2 + 2Н2О +2610 кДж выделилось 652, 5 кДж теплоты. Объём сгоревшего ацетилена равен
1) 11,2 л 2) 22,4 л 3) 44,8 л 4) 67,2 л
8. Какое выражение соответствует константе химического равновесия для данной реакции
N2+3H2 = 2NH3
1) Kc = [NH3]2/ [N2]+[H2]3 3) Кр = [NH3]2 / [N2][H2]
2) Кс = [NH3]2 / [N2][H2]3 4) Кс = []N2][H2]3/ [NH3]2
9. Как нужно изменить давление, чтобы реакция гемоглобина с кислородом
Hb + O2 «HbO2 была смещена вправо?
1) уменьшить давление 2) увеличить давление 3) давление не влияет
10. Какое значение константы равновесия соответствует данной реакции 2NO +O2 «2NO2
1) Kc= [NO2]2/ [NO][O2] 3) Kc= [NO][O2]/ [NO2]2
2) Kc= [NO2]2 / [NO]2[O2] 4) Kc= [NO2]/ [NO][O2]
11. Как нужно изменить давление реакции N2+3H2 «2 NH3, чтобы сместить равновесие вправо?
1) уменьшить 3) не изменять
2) увеличить 4) увеличить давление NH3
12. Будет ли влиять давление на смещение равновесия данной реакции H2 + Cl2 = 2 HCl?
1) будет 2) нет
3) сместит равновесие вправо 4) сместит равновесие влево
13. Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в обратном направлении?
1) DG0 < 0 2) DG0 > 0 3) DG0 = 0 4) DG0 = 1
14. Равновесие в реакции, уравнение которой СН4(г) + 4S(ж) ↔ СS2(г) + 2Н2S(г), ΔH<0, сместиться влево при ______.
1) понижении давления 3) дополнительном введении серы
2) понижении температуры 4) увеличении концентрации H2S
15. Будет ли протекать реакция в прямом направлении, если DG = 18 кДж/моль?
1) нет 2) химическое равновесие 3) будет
16. Система, в которой повышение давления и повышение температуры приведут к смещению равновесия в противоположных направлениях:
1) СO2(г) + C(т) ↔ 2СО(г), ΔН<0
2) J2(г) + 5 СО2(г) ↔ J2O5(т) + 5СО(г), ΔН>0
3) N2(г) + О2(г) ↔ 2 NO(г), ΔН>0
4) С2Н2(г) + 2Н2(г) ↔ С2Н6 (г), ΔН<0
17. Как нужно изменить давление, чтобы равнеовесие реакции гемоглобина с кислородом былаосмещено влево Hb + O2 «HbO2?
1) уменьшить давление 2) увеличить давление 3) давление не влияет
18. В реагирующей системе, уравнение которой NO(г) + Cl2(г) ↔ NOCl2(г) ΔH > 0, равновесие сместиться вправо при_____.
1) повышении давления 3) понижении температуры
2) использовании катализатора 4) повышении концентрации NOCl2
19. Для смещения равновесия в системе SO2(г)+Cl2(г) 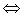 SO2Cl2(г), DH°<0 в сторону продуктов реакции необходимо_____,
SO2Cl2(г), DH°<0 в сторону продуктов реакции необходимо_____,
1) понизить температуру 3) понизить концентрацию SO2
2) понизить давление 4) ввести катализатор 5) повысить температуру
20. На состояние химического равновесия в системе 2SO2(г) + О2 (г) ↔2 SO3, ΔH0 < 0 не влияет____
1) катализатор 3) изменение температуры
2) изменение концентрации исходных веществ 4) изменение давления
21. Для нахождения 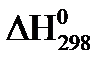 реакции
реакции 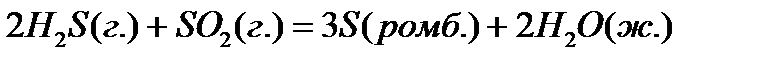 , следует воспользоваться формулой:
, следует воспользоваться формулой:
1) 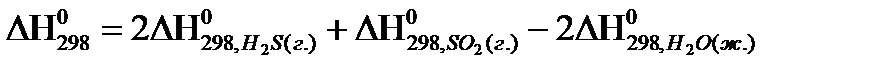
2) 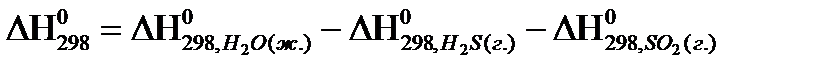
3) 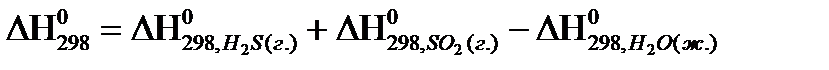
4) 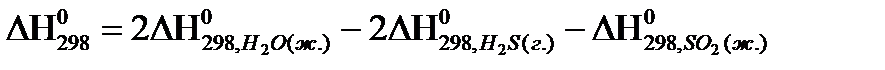
22. Для нахождения 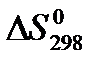 реакции
реакции 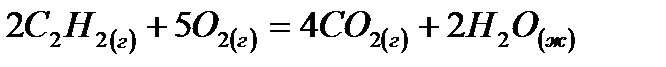 следует воспользоваться формулой: 1)
следует воспользоваться формулой: 1) 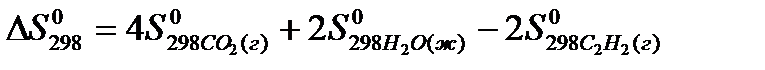
2) 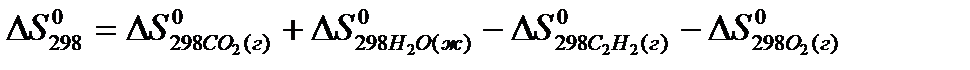
3) 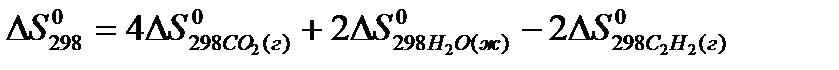
4) 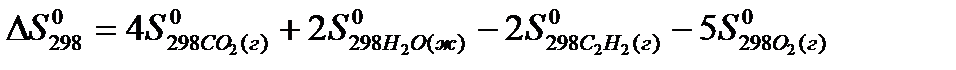
 2015-10-14
2015-10-14 1265
1265








