Разбавленные растворы неэлектролитов обладают рядом свойств (коллигативные свойства), количественное выражение которых зависит только от числа находящихся в растворе частиц растворенного вещества и от количества растворителя.
3.2.1 Осмотическое давление разбавленных растворов неэлектролитов.
Пример 1. Вычисление осмотического давления растворов.
Вычислите осмотическое давление раствора, содержащего в 1,4 л 63 г глюкозы 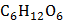 при ̊ С.
при ̊ С.
Решение. Осмотическое давление раствора определяют согласно закону Вант-Гоффа:
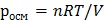
где n - количество растворенного вещества, моль; V - объем раствора, 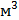 ;
;
R - молярная газовая постоянная, равная 8,3144 Дж/(моль ∙ К).
В 1,4 л раствора содержится 63 г глюкозы, молярная масса которой равна 180,16 г/моль. Следовательно, в 1,4 л раствора содержится n=63/180.16=0,35 моль глюкозы.
Осмотическое давление этого раствора глюкозы:
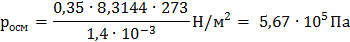
Пример 2. Определение молекулярной массы неэлектролита по осмотическому давлению раствора.
Рассчитайте молекулярную массу неэлектролита, если в 5 л раствора содержится 2,5 г неэлектролита. Осмотическое давление этого раствора равно 0,23∙ 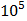 Па при 20 ̊ С.
Па при 20 ̊ С.
Решение. Заменив n выражение m/M, где m - масса растворенного вещества, а М - его молярная масса, получим
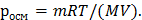
Отсюда молярная масса растворенного вещества равна
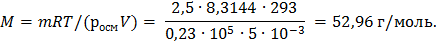
Следовательно, молекулярная масса неэлектролита равна 52,96
 2017-11-30
2017-11-30 695
695








