Образование из атомов молекул, молекулярных ионов, ионов, кристаллических, аморфных и других веществ сопровождается 1) уменьшением энергии по сравнению с невзаимодействующими атомами. 2)При этом минимальной энергии соответствует определенное расположение атомов друг относительно друга, которому отвечает существенное перераспределение электронной плотности.
Силы, удерживающие атомы в новых образованиях, получили обобщенное название «химическая связь». Важнейшие виды химической связи: ионная, ковалентная, металлическая
Согласно электронной теории валентности, химическая связь возникает за счет перераспределения электронов валентных орбиталей.
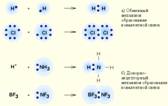
Ковалентная связь – наиболее общий вид химической связи, возникающий за счет обобществления электронной пары посредством обменного механизма, когда каждый из взаимодействующих атомов поставляет по одному электрону, или по донорно-акцепторному механизму, если электронная пара передается в общее пользование одним атомом (донором) другому атому (акцептору)
|
|
|
Ионная связь образуется при передаче электронов более электроотрицательному атому, т.е. за счёт электростатического притяжения разноимённо заряженных ионов. Ионы могут быть как простыми, так и сложными. Все ионные соединения имеют в твёрдом состоянии ионную кристаллическую решётку, в которой каждый ион окружён несколькими ионами противоположного знака.При этом все связи данного иона с соседними ионами равноценны, так что весь кристалл можно рассматривать как единую "молекулу". В ионных соединениях не происходит полного разделения зарядов на + и -, т.е. полного перехода электрона от одного атома к другому. Это можно объяснить взаимной поляризацией ионов, т.е. влиянием их друг на друга, которое приводит к деформации электронных оболочек. Поляризация ионов оказывает заметное влияние на свойства образуемых ими соединений (н-р: на диссоциацию солей в водных растворах
Металлическая связь возникает в результате частичной делокализации валентных электронов, которые достаточно свободно движутся в решетке металлов, электростатически взаимодействуя с положительно заряженными ионами. Силы связи не локализованы и не направлены, а делокализированные электроны обусловливают высокую тепло- и электропроводность.
 2018-01-21
2018-01-21 732
732








