Типы ОВР
Различают три типа окислительно-восстановительных реакций: межмолекулярные, внутримолекулярные, диспропорционирования. Межмолекулярные окислительно-восстановительные реакции - это реакции, в которых окислитель и восстановитель находятся в разных веществах. Рассмотренная выше реакция относится к этому типу. К внутримолекулярным относятся реакции, в которых окислитель и восстановитель находятся в одном и том же веществе.
2KCl+5O3-2 = 2KCl-1 + 3O20
восстановление Сl+5 + 6ē → Cl- ½2 Cl+5 - окислитель
окисление 2O-2 - 4ē → O20 ½3 O-2 - восстановитель
В реакциях диспропорционирования (самоокисления - самовосстановления) молекулы одного и того же вещества реагируют друг с другом как окислитель и как восстановитель.
3K2Mn+6O4 + 2H2O = 2KMn+7O4 + Mn+4O2 + 4KOH
окисление Mn+6 - ē → Mn+7 ½ 2 Mn+6 - восстановитель
восстановление Mn+6 + 2ē → Mn+4 ½ 1 Mn+6 - окислитель
В узлах кристаллической решетки металлов расположены положительно заряженные ионы, между которыми перемещаются валентные электроны. Эти электроны не имеют связи с отдельными ионами, а являются общими, принадлежащими всем ионам металла.
Если погрузить металл в воду или раствор его соли, то часть ионов металла, находящихся на поверхности, взаимодействует с полярными молекулами воды и переходит в раствор в виде гидратированных ионов. Вследствие этого раствор вблизи поверхности металла заряжается положительно, а в самом металле создается избыток электронов, придающих металлу отрицательный заряд.
Таким образом, на границе металл – раствор образуется двойной электрический слой и возникает определенный скачок потенциала. Разность потенциалов, которая возникает на границе металл – раствор, называется электродным потенциалом металла. Абсолютное значение электродного потенциала измерить невозможно. Поэтому электродные потенциалы определяют относительно стандартного водородного электрода, потенциал которого условно принят за ноль.
Устройство водородного электрода таково: платиновый электрод, покрытый мелкодисперсной платиной (платиновой чернью), погруженный в раствор серной кислоты с концентрацией ионов водорода 1 моль/л, обдувается струей газообразного водорода под давлением 101 кПа при температуре T = 298 K. Платиновый электрод, покрытый рыхлой платиной, адсорбирует атомарный водород. При насыщении платины водородом устанавливается равновесие:
Н2 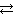 2Н. Когда такой электрод находится в растворе, содержащем ионы водорода Н+, то устанавливается следующее равновесие: Н
2Н. Когда такой электрод находится в растворе, содержащем ионы водорода Н+, то устанавливается следующее равновесие: Н 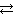 Н+ + ē. Суммарный процесс, происходящий на электроде, можно выразить уравнением:
Н+ + ē. Суммарный процесс, происходящий на электроде, можно выразить уравнением:
Pt, Н2 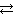 2Н
2Н 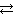 2Н+ + 2ē
2Н+ + 2ē
Электродный потенциал пары Pt, Н2 | 2Н+ условно принят за ноль и по отношению к нему измерены электродные потенциалы многих металлов.
Электродный потенциал, измеренный при стандартных условиях (т.е. при температуре 250С и концентрациях веществ, участвующих в электродном процессе, равных 1 моль/л) по отношению к стандартному водородному электроду, называется стандартным электродным потенциалом. Обозначается j0, измеряется в вольтах (В). Если условия отличаются от стандартных, то электродный потенциал рассчитывается по уравнению Нернста:
j = j0 + 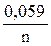 lgC
lgC
где j o - стандартный электродный потенциал, n – число электронов, участвующих в электродной реакции; C – концентрация ионов металла в растворе (моль/л).
 2014-01-31
2014-01-31 774
774








