1. Построить график зависимости объема выделившегося водорода от продолжительности испытания.
2. Рассчитать скорость коррозии (массовый показатель) за 100 мин. в г/м2∙час, при этом убыль массы образца Δm  рассчитать по закону эквивалентов, учитывая, что при растворении I г/экв металла выделяется 11,2 л водорода.
рассчитать по закону эквивалентов, учитывая, что при растворении I г/экв металла выделяется 11,2 л водорода.
3. Рассчитать глубинный показатель в мм/год и оценить стойкость образца по шкале баллов стойкости.
| Металл | 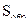 ,
м2 ,
м2
| 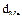 ,
г/см3 ,
г/см3
| τ, мин | Положение мениска, мл | 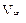 ,
мл ,
мл
| 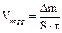 ,
г/м2∙час ,
г/м2∙час
|
Глубинный показатель_____
Балл стойкости____________
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
1. Объясните на конкретных примерах механизм химической и электрохимической коррозии.
2. Напишите электрохимические процессы, протекающие при нарушении: цинкового и оловянного покрытий на железе, эксплуатирующегося в атмосферных условиях.
3. Какие активаторы коррозии алюминия и железа вам известны?
4. Объясните влияние на коррозию металлов ионов Н+.
5. Какая алюминиевая пластинка корродирует интенсивнее в контакте:
а) с железом; б) с медью?
Работа № 18. Протекторная защита металлов от коррозии
Цель работы – знакомство с методами защиты металлов от коррозии. Изучение надежности протекторной защиты металлов. Определение радиуса действия цинкового протектора при защите стальных изделий при эксплуатации их в солевых растворах.
Оборудование и реактивы
1. Реохордный мост для измерения сопротивления раствора или кондуктометр для измерения электропроводности.
2. Стальной стержень с протектором (цинковой проволокой), закрепленным у основания стержня.
3. Большая пробирка.
4. Капельница с раствором красной кровяной соли.
5. Ячейка с платиновыми электродами.
6. Растворы поваренной соли NaCl (0,1%; 0,2%; 0,3%; 1,5%).
 2020-06-08
2020-06-08 360
360








