Тема: Летучие водородные соединения неметаллов.
Дата: 21.05.2020 (1 час)
Цель:
1. Обобщить знания о закономерностях изменения свойств водородных соединений неметаллов в периодах и группах в зависимости от их строения.
2. Проанализировать строение и свойства летучих водородных соединений неметаллов в зависимости от их положения в периодической таблице химических элементов Д.И. Менделеева.
Студенты должны знать: строение и свойства водородных соединений неметаллов, зависимость свойств от их положения в периодической системе химических элементов.
Студенты должны уметь: составлять формулы водородных соединений неметаллов, учитывая возможные степени окисления, и уравнения химических реакций.
План.
1. Получение летучих водородных соединений неметаллов.
2. Строение водородных соединений неметаллов.
3. Изменение кислотно-основные свойства водородных соединений по периоду.
4. Изменение кислотно-основные свойства водородных соединений по группе.
Посмотреть видеоурок https://www.youtube.com/watch?v=yOclCo8QtoA
|
|
|
Опорный конспект
В отличие от металлов неметаллы образуют газообразные водородные соединения. Их состав зависит от степени окисления неметаллов.
RH4 → RH3 → H2R → HR
Общим свойством всех неметаллов является образование летучих водородных соединений, в большинстве которых неметалл имеет низшую степень окисления. Среди приведенных формул веществ много тех, свойства, применение и получение которых вы изучали ранее: CH4, NH3, H2O, H2S, HCl.
Известно, что наиболее просто эти соединения можно получить непосредственно взаимодействием неметалла с водородом, то есть синтезом: 
Все водородные соединения неметаллов образованы ковалентными полярными связями, имеют молекулярное строение и при обычных условиях являются газами, кроме воды (жидкость). Для водородных соединений неметаллов характерно различное отношение к воде. Метан и силан в ней практически нерастворимы. Аммиак при растворении в воде образует слабое основание NH3 • H2O. При растворении в воде сероводорода, селеноводорода, теллуроводорода, а также галогеноводородов образуются кислоты с той же формулой, что и сами водородные соединения: H2S, H2Se, H2Te, HF, HCl, HBr, HI.
Если сравнить кислотно-основные свойства водородных соединений, образованных неметаллами одного периода, например, второго (NH3, H2O, HF) или третьего (PH3, H2S, HCl), то можно сделать вывод о закономерном усилении их кислотных свойств и, соответственно, ослаблении основных. Это, очевидно, связано с тем, что увеличивается полярность связи Э—Н (где Э — неметалл).
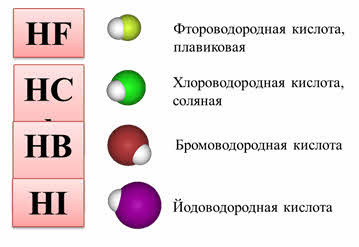
Кислотно-основные свойства водородных соединений неметаллов одной подгруппы также отличаются. Например, в ряду галогеноводородов HF, HCl, HBr, HI прочность связи Э—Н уменьшается, т. к. увеличивается длина связи. В растворах HCl, HBr, HI диссоциируют практически полностью — это сильные кислоты, причем их сила увеличивается от HF к HI. При этом HF относится к слабым кислотам, что обусловлено еще одним фактором — межмолекулярным взаимодействием, образованием водородных связей …H—F…H—F…. Атомы водорода связаны с атомами фтора F не только своей молекулы, но еще и соседней.
|
|
|
Обобщая сравнительную характеристику кислотно-основных свойств водородных соединений неметаллов, сделаем вывод об усилении кислотных и ослаблении основных свойств этих веществ по периодам и главным подгруппам с увеличением атомных номеров образующих их элементов.
По периоду в ПС химических элементов с увеличением порядкового номера элемента – неметалла усиливается кислотный характер водородного соединения.
SiH4 → PH3 → H2S → HCl
Кроме рассмотренных свойств, водородные соединения неметаллов в окислительно-восстановительных реакциях всегда проявляют свойства восстановителей, ведь в них неметалл имеет низшую степень окисления.
Например, водный раствор хлороводорода – проявляет кислотные свойства, поэтому реагирует со щелочами. Так, в реакции соляной кислоты с гидроксидом натрия образуется соль – хлорид натрия и вода. Водный раствор аммиака проявляет основные свойства, поэтому реагирует с кислотами. Так, в реакции аммиака с серной кислотой образуется сульфат аммония и вода.
Как было сказано, водородные соединения неметаллов проявляют восстановительные свойства, так как элемент-неметалл здесь в минимальной степени окисления. Например, в реакции сероводорода с хлором сероводород является восстановителем, потому что сера повышает свою степень окисления с минус двух до нуля.

Вопросы для самоконтроля:
1. Какие водородные соединения вам известны?
2. Какой тип химической связи в летучих водородных соединениях?
3. Какую степень окисления проявляет водород в этих соединения?
4. Как находится степень окисления других неметаллов в этих соединениях?
5. Почему соединения металлов с водородом нелетучие?
6. Какой тип химической связи в них?
 2020-06-29
2020-06-29 227
227







