2.
1.Влияние одноименных ионов снижает растворимость осадка (Ks. – остается постоянной)
2. Присутствие разноименных ионов увеличивает растворимость осадка (солевой эффект), это связано с изменением ионной силы раствора μ:
Ks = aAg+aCl- = fAg+CAg+ fCl-CCl-;
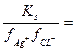 CAg+ CCl-;
CAg+ CCl-;
μ = ½ ΣCi Zi2
-lgf = 0,5 Z2 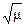
- lgf = 0,5 Z2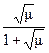
введение электролита μ↑ приводит к ↓f (-lgf) f↓ следовательно С↑.
При осаждении гидроксидов величина рН определяется величиной Ks, чем Ks меньше, тем при меньшем значении рН производится осаждение
| Fe(OH)3 | Ks = 10-38 | рН = 3,5 |
| Ni(OH)2 | Ks = 10-15 | рН = 9,8 |
| Mg(OH)2 | Ks = 10-10 | рН = 12,4 |
Кислоты (H2SiO3) осаждают из кислых растворов (рН 1-2)
Осаждение солей определяются природой аниона
при осаждении BaSO4 рН не имеет значение (осадок нерастворим в кислотах и щелочах)
BaCrO4 осаждается полнее при рН 4 – 5
ВаСО3 практически полностью осаждается при рН>8.
4. Температура с увеличением температуры растворимость увеличивается.
Растворимость осадков, стр.88, Васильев.
 2014-02-02
2014-02-02 570
570








