Уравнение Ван-дер-Ваальса можно записать в такой форме:
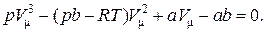 (17.7)
(17.7)
В зависимости от численных значений р и Т для данного газа это уравнение может иметь либо один, либо три действительных корня. Изотермы газа, построенные по уравнению (17.7):
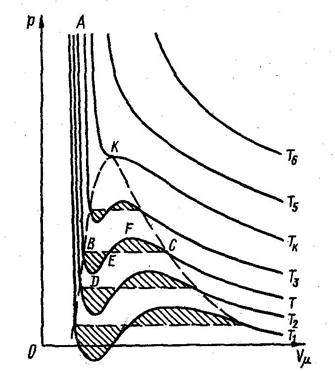
Рис.17.3
(Т1 <Т< Т2 <Tк <T3< Т4).
Опыты показывают, что некоторые состояния, соответствующие участкам BDEFC изотерм Ван-дер-Ваальса, реально осуществимы. Например, можно задержать кипение жидкости, тщательно удалив из нее механические примеси и производя нагревание в сосуде с гладкими стенками.
Участок BD соотв. перегретой жидкости, различным состояниям которой соответствуют точки (удалены все центры кипения).
Участок CF соотв. пересыщенному пару (удалены все центры конденсации).
Участок изотермы DEF реально неосуществим.
Изотермапри Т = Тк является критической, а точка К перегиба этой изотермы - критической точкой.
. Представим уравнение (17.7) в виде точного куба при p=р к и T=Тк:
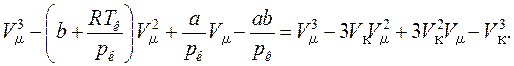
Это равенство тождественно выполняется, если коэффициенты при одинаковых степенях V равны в обеих его частях:
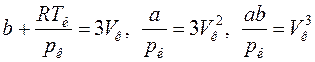 . (17.8)
. (17.8)
Пользуясь (17.8), получим выражения, которые связывают критические параметры с постоянными a и b. Из второго уравнения следует
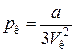 .
.
Подставив это выражение в третье уравнение, получим для критического объема
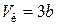 . (17.9)
. (17.9)
Тогда выражение для критического давления примет вид
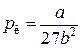 . (17.10)
. (17.10)
Подстановка выражений для 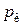 и
и 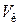 в первое уравнение дает
в первое уравнение дает
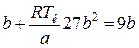 .
.
Отсюда получим формулу для критической температуры
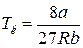 .
.
 2014-02-18
2014-02-18 1049
1049








