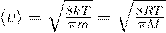
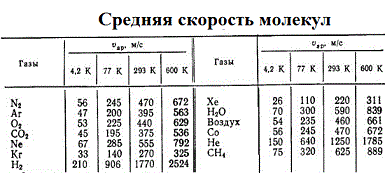
Для того чтоб понять, откуда же у нас получается эта формула, мы выведем среднюю скорость молекул. Вывод формулы начинается с закона изменения функции распределения молекул по скоростям 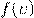 :
:
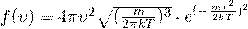
Что бы у нас получилась формула средней скорости молекул, надо взять интеграл этой функции от 0 до бесконечности:
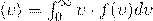
После взятия интеграла, у нас получается нужный нам результат — средняя скорость молекулы:
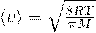
А если расписать универсальную газовую постоянную, как 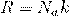 , и за одно молярную массу
, и за одно молярную массу 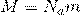 , то у нас получится:
, то у нас получится:
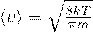
В Формуле мы использовали:
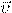 — Средняя квадратичная скорость молекул
— Средняя квадратичная скорость молекул
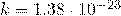 — Постоянная Больцмана
— Постоянная Больцмана
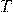 — Температура
— Температура
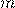 — Масса одной молекулы
— Масса одной молекулы
 — Универсальная газовая постоянная
— Универсальная газовая постоянная
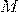 — Молярная масса
— Молярная масса
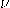 — Количество вещества
— Количество вещества
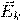 — Средняя кинетическая энергия молекул
— Средняя кинетическая энергия молекул
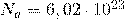 — Число Авогадро
— Число Авогадро
- 2.4. Прочие формулы по молекулярной физике -
Молярная масса вещества — Масса одного моля вещества. Отношение массы m вещества к его количеству n

Молярная масса обычно выражается в (грамм/моль). Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональна массе соответствующей структурной единицы, то есть относительной молекулярной массе (атомной массе) данного вещества.
|
|
|
Если рассмотреть пример: молярная масса атомарного водорода равна 1.0079 (г/моль), молекулярно водорода — 2.0158 (г/моль), молекулярно кислорода — 31.9988 (г/моль).
Поскольку масса любой молекулы равна сумме масс составляющих ее атомов, то относительная молекулярная масса равна сумме соответствующих относительных атомных масс.
Например, молекулярная масса воды, молекула которой содержит два атома водорода и один атом кислорода равна:
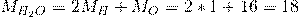 [г/моль]
[г/моль]
В Формуле мы использовали:
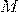 — Молярная масса вещества
— Молярная масса вещества
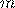 — Масса вещества
— Масса вещества
 — Колличество вещества
— Колличество вещества
 2014-02-24
2014-02-24 957
957








