| Строение и свойства газообразных, жидких и твердых тел | |||
| Газы | |||
| В газах расстояние между атомами или молекулами в среднем во много раз больше размеров самих молекул | 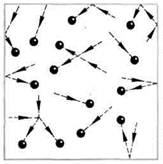
| ||
| Газы легко сжимаются, при этом уменьшается среднее расстояние между молекулами, но молекулы не сдавливают друг друга | 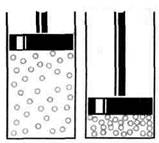
| ||
| Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема. | |||
| Жидкости | |||
| Молекулы жидкости находятся непосредственно друг возле друга. | 
| ||
| При попытке изменить объем жидкости (даже на малую величину) начинается деформация самих молекул. Для этого нужны очень большие силы. Этим и объясняется малая сжимаемость жидкостей. | 
| ||
| Жидкости текучи, т. е. не сохраняют своей формы. Объяснить это можно так. Если жидкость не течет, то перескоки молекул из одного оседлого положения в другое происходят с одинаковой частотой по всем направлениям. Внешняя сила заметно не меняет число перескоков молекул в секунду. Но перескоки молекул из одного оседлого положения в другое происходят преимущественно в направлении действия внешней силы. Вот почему жидкость течет и принимает форму сосуда. | 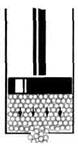
| ||
| Твердые тела | |||
| Атомы или молекулы твердых тел в отличие от атомов и молекул жидкостей колеблются около определенных положений равновесия. Правда, иногда молекулы меняют положение равновесия, но происходит это редко. Вот почему твердые тела сохраняют не только объем, но и форму. | 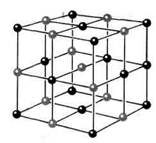
| ||
| Расстояния между молекулами твердых тел сравнимы с их размерами, поэтому любая попытка еще больше их сблизить вызывает возрастание сил взаимного отталкивания. Этим объясняется малая сжимаемость твердых тел. | |||
Зависимость давления газа от концентрации его молекул и температуры.
Уравнение ____________ можно записать иначе:
Поскольку _______________ ( концентрация молекул), получаем _____________,при __________________________________________________________________________________________________________
 Зная температуру, нетрудно вычислить среднюю кинетическую энергию. После этого легко вычислить и ср.скорость молекулы. А можно ли эту скорость измерить?
Зная температуру, нетрудно вычислить среднюю кинетическую энергию. После этого легко вычислить и ср.скорость молекулы. А можно ли эту скорость измерить?
 Если в уравнение ______________________________подставим______________, получим выражение среднего квадрата скорости
Если в уравнение ______________________________подставим______________, получим выражение среднего квадрата скорости
___________________________________________________________________
Квадратный корень из этой величины называется средней квадратичной скоростью
________________________________________________________________________
Средние скорости молекул превышают скорость звука и достигают сотен метров в секунду.
________________________________________________________________________________________________________________________________________________________Одни из опытов был предложен О. Штерном в 1920 году.
Пример Оценим скорость молекул в воздухе при комнатной температуре. Поскольку воздух состоит, в основном, из молекул азота и кислорода, для которых М=29 10-3 кг /моль, а комнатной температуре соответствует Т=300К получаем Vср.кв=500 м/с.
 2014-02-09
2014-02-09 990
990







